题目内容
有一包白色粉末,可能是CuSO4、CaCO3、BaCl2、Na2SO4、KOH、KCl中的一种或几种,为证明其组成,进行如图实验:
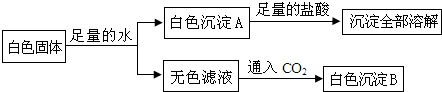
根据上述实验现象判断:
(1)白色沉淀A的化学式是 ;
(2)白色固体中一定不含 ,一定含有 ,可能含有 ;
(3)写出通入CO2生成白色沉淀的化学方程式 , .

根据上述实验现象判断:
(1)白色沉淀A的化学式是
(2)白色固体中一定不含
(3)写出通入CO2生成白色沉淀的化学方程式
考点:物质的鉴别、推断,盐的化学性质,书写化学方程式、文字表达式、电离方程式
专题:混合物组成的推断题
分析:根据硫酸铜在溶液中显蓝色,碳酸钙难溶于水,碳酸钙会与酸反应生成二氧化碳气体,硫酸钡沉淀难溶于酸,二氧化碳会与碱反应生成盐和水,碳酸根离子会与钡离子生成白色的碳酸钡沉淀等知识进行分析解答.
解答:解::硫酸铜溶于水得到蓝色溶液,题中加入足量的水溶解后是无色的溶液,所以在白色固体中一定不含硫酸铜,同时能形成白色沉淀的有碳酸钙,硫酸钠和氯化钡也可以反应生成白色沉淀,而白色沉淀能全部溶于稀硝酸,硫酸钠和氯化钡反应生成的硫酸钡不溶于稀硝酸,所以白色沉淀A为碳酸钙,所以硫酸钠和氯化钡最多含有一种,向无色滤液中通入CO2气体,得到白色沉淀,通入二氧化碳后产生了白色沉淀,根据题中所给的物质分析,这种白色沉淀只能是碳酸钡,但是二氧化碳不能与氯化钡直接反应生成沉淀,从而我们判断还应该有氢氧化钾,氢氧化钾与二氧化碳反应生成碳酸钾后,碳酸钾与氯化钡反应生成了碳酸钡沉淀,所以原白色粉末中还含有物质的是氯化钡、氢氧化钾,而混合物中是否含有氯化钾对实验现象不会造成影响,所以:
(1)白色沉淀A的化学式是:CaCO3;
(2)白色固体中一定不含:CuSO4、Na2SO4,一定含有:CaCO3、BaCl2、KOH,可能含有KCl;
(3)通入CO2生成白色沉淀的反应是氢氧化钾和二氧化碳反应生成碳酸钾和水,碳酸钾和氯化钡反应生成白色的碳酸钡沉淀和氯化钾,化学方程式为:2KOH+CO2=K2CO3+H2O,K2CO3+BaCl2=BaCO3↓+2KCl.
故答案为:(1)CaCO3;
(2)CuSO4、Na2SO4,CaCO3、BaCl2、KOH,KCl;
(3)2KOH+CO2=K2CO3+H2O,K2CO3+BaCl2=BaCO3↓+2KCl.
(1)白色沉淀A的化学式是:CaCO3;
(2)白色固体中一定不含:CuSO4、Na2SO4,一定含有:CaCO3、BaCl2、KOH,可能含有KCl;
(3)通入CO2生成白色沉淀的反应是氢氧化钾和二氧化碳反应生成碳酸钾和水,碳酸钾和氯化钡反应生成白色的碳酸钡沉淀和氯化钾,化学方程式为:2KOH+CO2=K2CO3+H2O,K2CO3+BaCl2=BaCO3↓+2KCl.
故答案为:(1)CaCO3;
(2)CuSO4、Na2SO4,CaCO3、BaCl2、KOH,KCl;
(3)2KOH+CO2=K2CO3+H2O,K2CO3+BaCl2=BaCO3↓+2KCl.
点评:在解此类题时,首先分析题中所给物质的性质,然后依据题中的现象确定各种物质的存在性,最后确定混合物的成分.

练习册系列答案
相关题目
推理是化学学习中常见的思维方法.下列推理正确的是( )
| A、碱性溶液能使酚酞试液变红,滴入酚酞试液后变红的溶液一定呈碱性 |
| B、酸碱发生中和反应生成盐和水,所以生成水的反应一定是中和反应 |
| C、酸能使石蕊试液变红,CO2也能使紫色的石蕊试液变红,所以CO2是酸 |
| D、溶液中有晶体析出,其溶质质量减小,所以溶质的质量分数一定减小 |
 透明聚酯玻璃钢可用于制造导弹的雷达罩和宇航员使用的氧气瓶,乙二醇(如图)是生产透明聚酯玻璃钢的原料之一.关于乙二醇的下列说法中,正确的是( )
透明聚酯玻璃钢可用于制造导弹的雷达罩和宇航员使用的氧气瓶,乙二醇(如图)是生产透明聚酯玻璃钢的原料之一.关于乙二醇的下列说法中,正确的是( )| A、乙二醇由碳、氢、氧三种原子构成 |
| B、乙二醇属于有机物 |
| C、乙二醇中碳元素含量最高 |
| D、乙二醇中碳、氢、氧三种元素的质量比为1:3:1 |


 2014年3月21日,继电、水实行阶梯计费后,国家发改委印发《关于建立健全居民生活用气阶梯价格制度的指导意见》,部署建立健全居民生活用气阶梯价格制度.建立阶梯气价的目的是
2014年3月21日,继电、水实行阶梯计费后,国家发改委印发《关于建立健全居民生活用气阶梯价格制度的指导意见》,部署建立健全居民生活用气阶梯价格制度.建立阶梯气价的目的是