题目内容
探究物质溶解时溶液温度的变化.
物质在溶解扩散的过程中,与溶剂的分子发生作用,通常都伴随着能量的变化.那么我们是否能直观地观察其中的能量变化呢?让我们来进行下面的实验探究.
【提出问题】当学完物质在水中的溶解以后,同学们议论开了:物质在溶解时,溶液的温度是否会发生变化?不同的物质溶解在水中时,溶液温度的变化情况是否一样?
【建立假设】甲组同学认为物质溶于水时溶液温度不会变化,而乙组同学认为溶液的温度会发生变化,于是他们进行了以下实验探究.
【实验探究】方案一:(1)取三只烧杯,分别加入50ml水,用温度计测量水的温度.(2)分别取一药匙氯化钠、硝酸铵、氢氧化钠加入上述三只烧杯中,用玻璃棒搅拌至固体完全溶解,测量溶液的温度.
(3)记录溶解前后液体温度的变化,填入下表中.
(4)把实验后的溶液倒入指定的容器内.
【讨论与分析】我们能否尽可能地利用生活中的用品探究物质溶解时吸热和放热现象?
方案二:用品:玻璃杯、小木片、蜡烛、火柴、氢氧化钠、硝酸铵化肥、水
设计实验:(完成实验探究中的表格)
【解释与结论】氯化钠溶解时,溶液的温度 ;硝酸铵溶解时,溶液的温度 ,试从微观角度分析原因 ;氢氧化钠溶解时,温度 .所以,物质溶于水形成溶液的过程中,通常伴随着能量变化.【反思与评价】比较两个探究实验方案,试着说出它们的优点或不足之处 .
物质在溶解扩散的过程中,与溶剂的分子发生作用,通常都伴随着能量的变化.那么我们是否能直观地观察其中的能量变化呢?让我们来进行下面的实验探究.
【提出问题】当学完物质在水中的溶解以后,同学们议论开了:物质在溶解时,溶液的温度是否会发生变化?不同的物质溶解在水中时,溶液温度的变化情况是否一样?
【建立假设】甲组同学认为物质溶于水时溶液温度不会变化,而乙组同学认为溶液的温度会发生变化,于是他们进行了以下实验探究.
【实验探究】方案一:(1)取三只烧杯,分别加入50ml水,用温度计测量水的温度.(2)分别取一药匙氯化钠、硝酸铵、氢氧化钠加入上述三只烧杯中,用玻璃棒搅拌至固体完全溶解,测量溶液的温度.
(3)记录溶解前后液体温度的变化,填入下表中.
| 溶质 温度 | 溶解前水的温度/℃ | 溶解后溶液的温度/℃ | 温度的变化/℃ |
| 氯化钠 | 19 | 19.5 | |
| 硝酸铵 | 19 | 8 | |
| 氢氧化钠 | 19 | 31 |
【讨论与分析】我们能否尽可能地利用生活中的用品探究物质溶解时吸热和放热现象?
方案二:用品:玻璃杯、小木片、蜡烛、火柴、氢氧化钠、硝酸铵化肥、水
设计实验:(完成实验探究中的表格)
| 实验步骤 | 实验现象 | 解释与结论 | |
| 探究氢氧化钠溶于水后溶液的温度变化 | 点燃蜡烛,杯底部用石蜡油粘上小木片,蜡油凝固后向玻璃杯中放入50ml水,加入2药匙氢氧化钠固体 | ||
| 探究硝酸铵溶于水后温度变化 | |
考点:溶解时的吸热或放热现象
专题:溶液、浊液与溶解度
分析:方案一:根据记录溶解前后液体温度,分析温度的变化;
方案二:根据氢氧化钠和硝酸铵溶解吸放热现象设计验证方案;
【解释与结论】根据方案一得出结论,
【反思与评价】根据两方案,操作分析优点或不足之处.
方案二:根据氢氧化钠和硝酸铵溶解吸放热现象设计验证方案;
【解释与结论】根据方案一得出结论,
【反思与评价】根据两方案,操作分析优点或不足之处.
解答:解:方案一:(3)对比记录溶解前后液体温度,可知氯化钠:升高0.5℃;硝酸铵:降低11℃氢氧化钠:升高12℃
方案二:氢氧化钠溶于水放热,可使石蜡融化,小木片脱落;
硝酸铵溶于水吸热,可以用小木片上洒一些水,再放上一个玻璃杯,向玻璃杯中倒入50ml水,加入2药匙硝酸铵,小木片与玻璃杯粘在一起的方法验证;
【解释与结论】由实验可知:氯化钠溶解时,溶液的温度基本不变;硝酸铵溶解时,铵根离子和硝酸根离子在水分子的作用下向水中扩散时吸收的热量大于与 水分子结合成水合离子时放出的热量,所以温度降低;氢氧化钠溶解时,温度升高.
【反思与评价】方案一中用到了温度计,能准确测量物质溶于水后溶液的温度变化情况;方案二中生活中的物品做实验,但只有物质溶解时温度变化花较大的变化,才有明显的实验现象,该方案有一定的局限性.
故答案为:方案一:(3)
方案二:
【解释与结论】基本不变;降低;铵根离子和硝酸根离子在水分子的作用下向水中扩散时吸收的热量大于与水分子结合成水合离子时放出的热量,所以温度降低;升高
【反思与评价】方案一中用到了温度计,能准确测量物质溶于水后溶液的温度变化情况;方案二中生活中的物品做实验,但只有物质溶解时温度变化花较大的变化,才有明显的实验现象,该方案有一定的局限性.
方案二:氢氧化钠溶于水放热,可使石蜡融化,小木片脱落;
硝酸铵溶于水吸热,可以用小木片上洒一些水,再放上一个玻璃杯,向玻璃杯中倒入50ml水,加入2药匙硝酸铵,小木片与玻璃杯粘在一起的方法验证;
【解释与结论】由实验可知:氯化钠溶解时,溶液的温度基本不变;硝酸铵溶解时,铵根离子和硝酸根离子在水分子的作用下向水中扩散时吸收的热量大于与 水分子结合成水合离子时放出的热量,所以温度降低;氢氧化钠溶解时,温度升高.
【反思与评价】方案一中用到了温度计,能准确测量物质溶于水后溶液的温度变化情况;方案二中生活中的物品做实验,但只有物质溶解时温度变化花较大的变化,才有明显的实验现象,该方案有一定的局限性.
故答案为:方案一:(3)
| 溶质 温度 | 溶解前水的温度/℃ | 溶解后溶液的温度/℃ | 温度的变化/℃ |
| 氯化钠 | 19 | 19.5 | 升高0.5 |
| 硝酸铵 | 19 | 8 | 降低11 |
| 氢氧化钠 | 19 | 31 | 升高12 |
| 实验步 骤 | 实验现象 | 解释与结论 | |
| 小木片脱落 | 氢氧化钠 溶于水时放出大量的热 | ||
| 在小木片上洒一些水,再放上一个玻璃杯,向玻璃杯中倒入50ml水,加入2药匙硝酸铵 | 小木片与玻璃杯粘在一起 | 硝酸铵溶于水时吸收大量的热 |
【反思与评价】方案一中用到了温度计,能准确测量物质溶于水后溶液的温度变化情况;方案二中生活中的物品做实验,但只有物质溶解时温度变化花较大的变化,才有明显的实验现象,该方案有一定的局限性.
点评:本题难度不大,掌握常见物质溶于水的吸热与放热现象、温度变化情况是正确解答本题的关键.

练习册系列答案
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案
相关题目
下面几种实验装置或操作正确的是( )
A、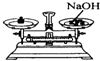 称量氢氧化钠 |
B、 滴加液体 |
C、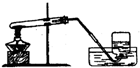 实验室制取氧气 |
D、 稀释浓硫酸 |
某同学做实验时记录了下列实验现象,其中正确的是( )
| A、红磷在空气中燃烧,产生大量白色烟雾 |
| B、细铁丝在氧气中剧烈燃烧,火星四射,有黑色固体生成 |
| C、少量高锰酸钾固体溶于水,得到绿色溶液 |
| D、硫在氧气中燃烧产生淡蓝色火焰 |
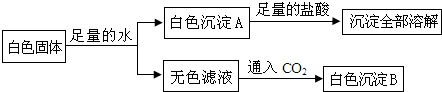
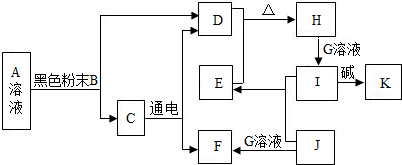
 某化学兴趣小组在实验室发现了一瓶标签受到腐蚀(如右图所示)的溶液,他们对此产生了兴趣.
某化学兴趣小组在实验室发现了一瓶标签受到腐蚀(如右图所示)的溶液,他们对此产生了兴趣.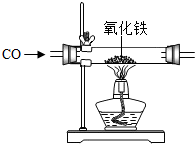 化学与人类生活生产息息相关,请用化学知识解答下列问题.
化学与人类生活生产息息相关,请用化学知识解答下列问题.