题目内容
 透明聚酯玻璃钢可用于制造导弹的雷达罩和宇航员使用的氧气瓶,乙二醇(如图)是生产透明聚酯玻璃钢的原料之一.关于乙二醇的下列说法中,正确的是( )
透明聚酯玻璃钢可用于制造导弹的雷达罩和宇航员使用的氧气瓶,乙二醇(如图)是生产透明聚酯玻璃钢的原料之一.关于乙二醇的下列说法中,正确的是( )| A、乙二醇由碳、氢、氧三种原子构成 |
| B、乙二醇属于有机物 |
| C、乙二醇中碳元素含量最高 |
| D、乙二醇中碳、氢、氧三种元素的质量比为1:3:1 |
考点:化学式的书写及意义,有机物与无机物的区别,元素质量比的计算,元素的质量分数计算
专题:化学用语和质量守恒定律
分析:A、根据乙二醇的微观构成进行分析判断.
B、含有碳元素的化合物叫有机化合物,简称有机物.
C、根据化合物中元素的质量分数=
×100%,进行分析判断.
D、根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析判断.
B、含有碳元素的化合物叫有机化合物,简称有机物.
C、根据化合物中元素的质量分数=
| 相对原子质量×原子个数 |
| 相对分子质量 |
D、根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析判断.
解答:解:A、乙二醇是由乙二醇分子构成的,乙二醇分子是由碳原子、氢原子、氧原子构成的,故选项说法错误.
B、乙二醇是含碳元素的化合物,属于有机物,故选项说法正确.
C、乙二醇中碳原子的相对原子质量之和为12×2=24,氢原子的相对原子质量之和为1×6=6,氧原子的相对原子质量之和为16×2=32,氧元素的相对原子质量之和最大,则氧元素的质量分数最大,故选项说法错误.
D、乙二醇中碳、氢、氧元素的质量比为(12×2):(1×6):(16×2)≠1:3:1,故选项说法错误.
故选:B.
B、乙二醇是含碳元素的化合物,属于有机物,故选项说法正确.
C、乙二醇中碳原子的相对原子质量之和为12×2=24,氢原子的相对原子质量之和为1×6=6,氧原子的相对原子质量之和为16×2=32,氧元素的相对原子质量之和最大,则氧元素的质量分数最大,故选项说法错误.
D、乙二醇中碳、氢、氧元素的质量比为(12×2):(1×6):(16×2)≠1:3:1,故选项说法错误.
故选:B.
点评:本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.

练习册系列答案
 走进文言文系列答案
走进文言文系列答案
相关题目
下面几种实验装置或操作正确的是( )
A、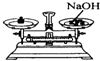 称量氢氧化钠 |
B、 滴加液体 |
C、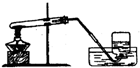 实验室制取氧气 |
D、 稀释浓硫酸 |
下列变化中,属于化学变化的是( )
| A、酒精挥发 | B、玻璃破碎 |
| C、食物变质 | D、干冰升华 |
下列物质由离子构成的是( )
| A、铁 | B、硫酸铜 | C、氧气 | D、金刚石 |
下列各组实验中,未用控制变量法进行对比实验的是( )
A、 |
B、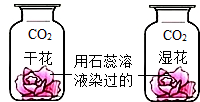 |
C、 |
D、 |
某同学做实验时记录了下列实验现象,其中正确的是( )
| A、红磷在空气中燃烧,产生大量白色烟雾 |
| B、细铁丝在氧气中剧烈燃烧,火星四射,有黑色固体生成 |
| C、少量高锰酸钾固体溶于水,得到绿色溶液 |
| D、硫在氧气中燃烧产生淡蓝色火焰 |
 如图是某粒子的结构示意图,回答下列问题:
如图是某粒子的结构示意图,回答下列问题: