题目内容
5.如图为某反应的微观示意图,其中“ ”和“
”和“ ”表示不同元素的原子.下列说法正确的是( )
”表示不同元素的原子.下列说法正确的是( )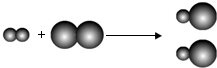
| A. | 反应前后元素化合价都没变 | B. | 该反应属于化合反应 | ||
| C. | 反应前后分子种类没有改变 | D. | 参加反应的两种分子个数比为1:2 |
分析 根据反应的微观示意图,分析反应前后原子的数目、分子的种类的变化;分析反应的类型及参加反应的两种分子个数比.
解答 解:由反应的微观示意图可知:
A、反应前的两种物质都是单质,化合价都是0,变成化合物元素的化合价发生了改变,故A错误;
B、该反应由两种物质生成了一种物质,属于化合反应,故B正确;
C、反应前后分子种类发生了改变.故C错误;
D、参加反应的两种分子个数比为1:1,故D错误.
故选B.
点评 本题属于微观示意图的考查,解答本题的关键是要充分理解图中的信息,只有这样才能对问题做出正确的判断.

练习册系列答案
相关题目
15.根据物质的组成.小明将部分物质分为甲、乙两类(如表所示).下列对分类结果判断正确的是( )
| 类别 | 物质 |
| 甲 | 硫酸、碳酸钠 |
| 乙 | 氧气、铜 |
| A. | 甲为酸,乙为单质 | B. | 甲为化合物,乙为单质 | ||
| C. | 甲为氧化物,乙为金属 | D. | 甲为盐,乙为氧化物 |
16.下列各项为小明同学记录的实验现象,与事实相符的是( )
| A. | 铁丝在空气中燃烧时,火星四射,有黑色固体 | |
| B. | 加碘盐中混入面粉时变成蓝色 | |
| C. | 高温加热时,黄铜比铜更易熔化 | |
| D. | 镁在空气中燃烧时,生成黑色固体 |
13.下列实验操作规范的是( )
| A. |  装药品 | B. |  闻气体气味 | ||
| C. |  滴管用后不洗插回原瓶 | D. |  用力塞紧橡皮塞 |
10.除去下列各组物质中的杂质,所用试剂和方法均正确的是( )
| 物质 | 杂质 | 除杂所用试剂和方法 | |
| A | CO2 | CO | 通入O2,点燃 |
| B | 二氧化碳 | 氯化氢气体 | 通过氢氧化钠溶液 |
| C | Cu(NO3)2溶液 | AgNO3溶液 | 加入过量的铜粉,过滤 |
| D | NaCl | Na2CO3 | 先加入适量澄清的石灰水,再过滤 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
14.下列说法正确的是( )
| A. | 浓硫酸露置在空气中溶质的质量分数会变大 | |
| B. | 某固体中加入稀盐酸产生无色气体,证明该固体一定含有碳酸根离子 | |
| C. | 用适量的稀盐酸除去NaCl溶液中的Na2CO3 | |
| D. | 通过溶解、过滤的方法除去生石灰中的碳酸钙 |
15.甲烷(CH4)气体难溶于水,不与浓硫酸、硫酸铜、碱石灰(氢氧化钠和氧化钙的固体混合物)、澄清石灰水等起反应.甲烷具有还原性,在加热条件下与氧化铜发生反应,生成铜、水和二氧化碳.
某化学小组为验证甲烷的组成,设计了如图所示实验. 该实验装置气密性良好,实验中所用试剂均足量.

已知装置 B、C、D、E中分别盛有浓硫酸、白色无水CuSO4固体、碱石灰、澄清石灰水,而且已知白色无水CuSO4固体遇水会变蓝色.
(1)实验步骤:
Ⅰ.通人甲烷气体.
Ⅱ.点燃酒精灯加热,反应一段时间后,停止加热.
Ⅲ.继续通甲烷至玻璃管冷却.
(2)有关现象:
①A中黑色固体变红色;②C中未见变蓝色;③E中未见出现浑浊.
(3)有关数据:
请回答下列问题:
(1)实验室若用无水醋酸钠固体和碱石灰混合加热制取甲烷,则发生装置类型与C相同.
A.用石灰石与稀盐酸制二氧化碳 B.用过氧化氢制氧气 C.用高锰酸钾制氧气
(2)甲烷还原氧化铜的化学方程式为CH4+4CuO$\frac{\underline{\;\;△\;\;}}{\;}$4Cu+2H2O+CO2.
(3)实验过程中通入甲烷的作用各不相同.步骤Ⅰ是排尽除去装置中的空气; 步骤Ⅱ是还原氧化铜;步骤Ⅲ是将生成的气体全部排出,减小实验误差.
(4)请根据该实验数据列计算式,证明甲烷中不含氧元素.相关计算式为108.0g-106.4g=(212.9g-212.og)×$\frac{16}{18}$×100%+(131.1g-131.0g)×$\frac{32}{44}$×100%=1.6g.
某化学小组为验证甲烷的组成,设计了如图所示实验. 该实验装置气密性良好,实验中所用试剂均足量.

已知装置 B、C、D、E中分别盛有浓硫酸、白色无水CuSO4固体、碱石灰、澄清石灰水,而且已知白色无水CuSO4固体遇水会变蓝色.
(1)实验步骤:
Ⅰ.通人甲烷气体.
Ⅱ.点燃酒精灯加热,反应一段时间后,停止加热.
Ⅲ.继续通甲烷至玻璃管冷却.
(2)有关现象:
①A中黑色固体变红色;②C中未见变蓝色;③E中未见出现浑浊.
(3)有关数据:
| A中玻璃管及物质总质量/g | B装置及物质总质量/g | D装置及物质总质量/g | |
| 反应前 | 108.0 | 212.0 | 131.0 |
| 反应后 | 106.4 | 212.9 | 132.1 |
(1)实验室若用无水醋酸钠固体和碱石灰混合加热制取甲烷,则发生装置类型与C相同.
A.用石灰石与稀盐酸制二氧化碳 B.用过氧化氢制氧气 C.用高锰酸钾制氧气
(2)甲烷还原氧化铜的化学方程式为CH4+4CuO$\frac{\underline{\;\;△\;\;}}{\;}$4Cu+2H2O+CO2.
(3)实验过程中通入甲烷的作用各不相同.步骤Ⅰ是排尽除去装置中的空气; 步骤Ⅱ是还原氧化铜;步骤Ⅲ是将生成的气体全部排出,减小实验误差.
(4)请根据该实验数据列计算式,证明甲烷中不含氧元素.相关计算式为108.0g-106.4g=(212.9g-212.og)×$\frac{16}{18}$×100%+(131.1g-131.0g)×$\frac{32}{44}$×100%=1.6g.

