题目内容
15.根据物质的组成.小明将部分物质分为甲、乙两类(如表所示).下列对分类结果判断正确的是( )| 类别 | 物质 |
| 甲 | 硫酸、碳酸钠 |
| 乙 | 氧气、铜 |
| A. | 甲为酸,乙为单质 | B. | 甲为化合物,乙为单质 | ||
| C. | 甲为氧化物,乙为金属 | D. | 甲为盐,乙为氧化物 |
分析 酸是电离时电离出的阳离子全部是氢离子的化合物;由金属离子和酸根离子构成的化合物属于盐;由一种元素组成的纯净物是单质;由不同元素组成的纯净物是化合物;氧化物是指由两种元素组成并且一种元素是氧元素的化合物,据此分析.
解答 解:甲:硫酸属于化合物中的酸,碳酸钠属于化合物的盐;
乙:氧气、铜都是由一种元素组成的纯净物,都属于单质;
A、由上分析可知,甲为化合物,乙为单质,故错误;
B、由上分析可知,甲为化合物,乙为单质,故正确;
C、由上分析可知,甲中没有氧化物,乙中的铜为金属,氧气不是金属,故错误;
D、由上分析可知,甲中的碳酸钠是盐,而硫酸不是盐,乙中没有氧化物,故错误.
故选B.
点评 本题考查物质的分类应用,注意物质组成的分析,概念的实质理解,题目较简单.

练习册系列答案
相关题目
5.下列防锈措施合理的是( )
| A. | 经常用水冲洗自行车链条 | B. | 用过的菜刀及时用盐水清洗 | ||
| C. | 用“钢丝球”打磨铝锅表面 | D. | 在铁制暖片上刷油漆 |
6.工业上常用氧化黄铁矿的方法来制取硫酸亚铁,从而获取绿矾(FeSO4•7H2O).氧化黄铁矿的方程式为:2X+7O2+2H2O$\frac{\underline{\;高温\;}}{\;}$2FeSO4+2H2SO4,则黄铁矿的化学式为( )
| A. | FeS | B. | Fe2(SO4)3 | C. | FeS2 | D. | FeSO3 |
20.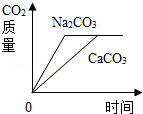 将等质量的CaCO3(块状)和Na2CO3(粉末),分别浸入一定量10%盐酸和10%硫酸溶液中,产生CO2的质量随时间变化曲线如图所示,下列说法正确的是( )
将等质量的CaCO3(块状)和Na2CO3(粉末),分别浸入一定量10%盐酸和10%硫酸溶液中,产生CO2的质量随时间变化曲线如图所示,下列说法正确的是( )
 将等质量的CaCO3(块状)和Na2CO3(粉末),分别浸入一定量10%盐酸和10%硫酸溶液中,产生CO2的质量随时间变化曲线如图所示,下列说法正确的是( )
将等质量的CaCO3(块状)和Na2CO3(粉末),分别浸入一定量10%盐酸和10%硫酸溶液中,产生CO2的质量随时间变化曲线如图所示,下列说法正确的是( )| A. | CaCO3一定没有剩余 | B. | 消耗HCl与H2SO4的质量比为1:1 | ||
| C. | 消耗CaCO3与Na2CO3的质量比为1:1 | D. | 反应产生水的质量相等 |
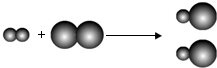
5.如图为某反应的微观示意图,其中“ ”和“
”和“ ”表示不同元素的原子.下列说法正确的是( )
”表示不同元素的原子.下列说法正确的是( )
 ”和“
”和“ ”表示不同元素的原子.下列说法正确的是( )
”表示不同元素的原子.下列说法正确的是( )
| A. | 反应前后元素化合价都没变 | B. | 该反应属于化合反应 | ||
| C. | 反应前后分子种类没有改变 | D. | 参加反应的两种分子个数比为1:2 |
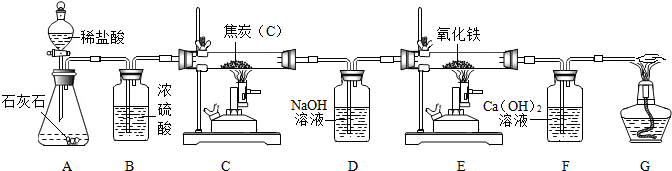
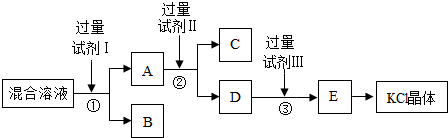
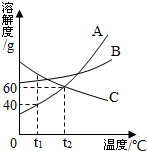 如图是A、B、C三种物质的溶解度曲线.请回答:
如图是A、B、C三种物质的溶解度曲线.请回答: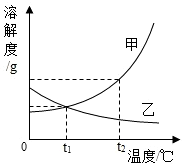 如图是甲、乙两种固体物质的溶解度曲线.
如图是甲、乙两种固体物质的溶解度曲线.