题目内容
5.将Na2SO4和Na2CO3固体混合物24.8g与179.6g硫酸恰好完全反应,气体完全逸出后溶液质量为200g.试计算:(1)产生气体的质量为4.4g
(2)反应后所得溶液溶质的质量分数.
分析 (1)根据碳酸钠与硫酸反应生成了二氧化碳,分析图象,根据质量守恒定律,物质的总质量减少的质量就是生成的二氧化碳的质量;
(2)根据碳酸钠与硫酸的反应,由二氧化碳的质量可求出反应的碳酸钠的质量、生成的硫酸钠的质量;根据碳酸钠的质量可求出原混合物中硫酸钠的质量,即可求出反应后溶液中溶质硫酸钠的质量.
解答 解:
(1)由于碳酸钠与硫酸反应生成了二氧化碳,由质量守恒定律和图象可知,生成二氧化碳的质量为:24.8g+179.6g-200g=4.4g;
(2)设固体混合物中碳酸钠的质量为x,生成的硫酸钠的质量为y
Na2CO3+H2SO4=Na2SO4+H2O+CO2↑
106 142 44
x y 4.4g
$\frac{106}{x}=\frac{142}{y}=\frac{44}{4.4g}$
解得x=10.6g y=14.2g
原混合物中硫酸钠的质量为:24.8g-10.6g=14.2g
所得溶液中溶质的质量分数=$\frac{14.2g+14.2g}{200g}$×100%=14.2%
答案:
(1)4.4
(2)所得溶液中溶质的质量分数为14.2%
点评 本题利用图表及反应方程式来分析和解决化学计算中的有关问题,要求学生有较强的识图能力和数据分析能力.

练习册系列答案
相关题目
15.据报道,一个国际科研团队实验证实了第117号元素的存在.科学家确认它的依据是( )
| A. | 质子数 | B. | 中子数 | C. | 相对原子质量 | D. | 最外层电子数 |
16.下列物质由原子直接构成的是( )
| A. | 干冰 | B. | 汞 | C. | 氯化钠 | D. | 氧气 |
20.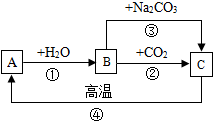 A、B、C是三种常见的含钙化合物.它们之间有如图所示的转化关系(部分产物略去).下列说法不正确的是( )
A、B、C是三种常见的含钙化合物.它们之间有如图所示的转化关系(部分产物略去).下列说法不正确的是( )
 A、B、C是三种常见的含钙化合物.它们之间有如图所示的转化关系(部分产物略去).下列说法不正确的是( )
A、B、C是三种常见的含钙化合物.它们之间有如图所示的转化关系(部分产物略去).下列说法不正确的是( )| A. | A物质的化学式是:CaO | |
| B. | B物质的俗称是:熟石灰或(消石灰) | |
| C. | C物质的名称是:水 | |
| D. | B物质在农业生产中的一种用途:中和酸性土壤 |
10.下列有关碳和碳的氧化物的说法中错误的是( )
| A. | 石墨有良好的导电性,可用于制造干电池 | |
| B. | 干冰(固态二氧化碳)升华时吸热,可用于灭火,降低可燃物的着火点 | |
| C. | 金刚石是天然最硬的非金属单质,可制成钻石 | |
| D. | 一氧化碳都具有还原性,可用于冶铁 |
14.化学基本概念是学好化学的基础.对下列有关概念的认识正确的是( )
| A. | 原子是最小的微粒,不可再分 | |
| B. | 塑料、合成纤维和合成橡胶属于合成材料 | |
| C. | 均一、稳定的液体一定是溶液 | |
| D. | 中和反应是指能够生成盐和水的反应 |
15.除去下列各组物质中的少量杂质,所用方法正确的是( )
| 选项 | 物质 | 杂质 | 除杂方法 |
| A | Cu | CuO | 用足量稀盐酸溶解后过滤,并洗净和干燥所得固体 |
| B | CaO | Ca(OH)2 | 加入足量的稀盐酸 |
| C | H2 | CO | 通入O2,点燃 |
| D | O2 | H2O | 通过浓硫酸洗气 |
| A. | A | B. | B | C. | C | D. | D |

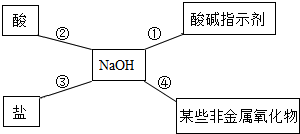 完成下列各题:
完成下列各题: