题目内容
17. 完成下列各题:
完成下列各题:(1)从某农田里取回一份土壤样品进行检测,结果pH<7,从经济和可行方面考虑,要改良此土壤,应向农田里施加Ca(OH)2(填化学式).
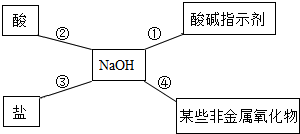
(2)如图总结了NaOH的性质:
Ⅰ.反应①发生的变化是化学变化(填“物理变化”或“化学变化”).
Ⅱ.依据反应④说明NaOH必须密封保存,否则在空气中要变质.写出NaOH在空气中变质的化学方程式CO2+2NaOH=Na2CO3+H2O.
Ⅲ.为了验证反应③能够发生,你选择的物质是C.
A.Na2CO3 B.HCl C.FeCl3 D.Ba(NO)2
(3)除去KCl溶液中少量的MgCl2,向混合液中加入适量KOH,过滤,发生反应的化学方程式是2KOH+MgCl2=Mg(OH)2↓+2KCl.
分析 (1)根据“酸碱中和反应“和“经济和可行”来选择需要添加的物质;
(2)Ⅰ.根据化学变化的实质进行分析;
Ⅱ.根据氢氧化钠变质是因为氢氧化钠与空气中的二氧化碳反应进行分析;
III.根据复分解反应的条件:必须有水、沉淀或气体生成进行分析;
(3)根据除杂的原则进行分析.
解答 解:(1)改良此土壤的酸性,一般加入熟石灰,故填:Ca(OH)2;
(2)Ⅰ.无色酚酞试液遇碱变成红色,遇酸变蓝色,生成了新物质,所以该变化属于化学变化;
Ⅱ.氢氧化钠变质是因为氢氧化钠与空气中的二氧化碳反应生成碳酸钠和水,反应的化学方程式为:CO2+2NaOH=Na2CO3+H2O;
III.氢氧化钠与盐反应属于复分解反应,复分解反应的条件:必须有水、沉淀或气体生成.
A.Na2CO3和氢氧化钠不反应,故A错误;
B.HCl是酸,不符合题意,故B错误;
C.FeCl3和NaOH反应生成氢氧化铁沉淀,满足复分解反应的条件,故C正确;
D.Ba(NO3)2和氢氧化钠不能满足复分解反应的条件,所以不反应,故D错误;
故选:C.
(3)除去KCl溶液中少量的MgCl2,向混合液中加入适量氢氧化钾,过滤,发生反应的化学方程式是:2KOH+MgCl2=2KCl+Mg(OH)2↓.
故答案为:(1)Ca(OH)2;
(2)Ⅰ、化学变化;
Ⅱ、2NaOH+CO2=Na2CO3+H2O;
Ⅲ、C;
(3)KOH,2KOH+MgCl2=2KCl+Mg(OH)2↓.
点评 本题考查酸碱盐的性质及利用性质除去物质中混有的杂质,是常见习题,考查学生考虑问题的全面性,尤其注意在除杂时不要引入新的杂质.

练习册系列答案
 导学全程练创优训练系列答案
导学全程练创优训练系列答案
相关题目
7.青砖烧制工艺中,有一步重要的反应:H2+Fe2O3=2X+H2O,其中X的化学式为( )
| A. | Fe | B. | FeO | C. | Fe3O4 | D. | O2 |
12.下列制取Fe2(SO4)3溶液的方案中,从反应原理和产物纯度考虑最佳的是( )
| A. | 过量的Fe粉与稀硫酸反应,过滤 | B. | 过量的Fe粉与CuSO4溶液反应,过滤 | ||
| C. | 过量的稀硫酸与Fe2O3反应 | D. | 过量的Fe2O3与稀硫酸反应,过滤 |
2.下列示意图所示原子,最有可能属于金属元素原子的是( )
| A. | 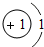 | B. | 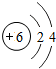 | C. | 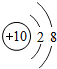 | D. | 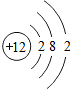 |
9.分类是学习化学的方法之一.下列物质分类错误的是( )
| A. | 水银:金属 | B. | 纯碱:碱 | C. | 空气:混合物 | D. | 干冰:氧化物 |
6.下列除去杂质的方法中正确的是( )
| 选项 | 物质 | 杂质 | 除杂质的方法 |
| A | NaCl溶液 | Na2CO3 | 适量硝酸钙溶液、过滤 |
| B | KOH溶液 | KCl | 适量稀盐酸 |
| C | CaCl2溶液 | 稀盐酸 | 过量碳酸钙、过滤 |
| D | O2 | CO | 通过灼热的氧化铜 |
| A. | A | B. | B | C. | C | D. | D |
7.厨房中物质加入适量水后不能形成溶液的是( )
| A. | 食盐 | B. | 蔗糖 | C. | 植物油 | D. | 纯碱 |