题目内容
做硫在氧气中燃烧的实验时,在集气瓶内放了少量水来吸收SO2,实验结束后,集气瓶内仍残留一定量的SO2.围绕如何处理这些SO2的问题,同学们进行了相关探究.
【提出问题】SO2是形成酸雨的主要物质.由此想到,选用氢氧化钠等碱性溶液吸收SO2,效果会怎样?
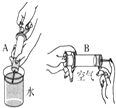
【设计与实验】用两套完全相同的装置做对比实验(SO2不溶于植物油也不与其反应),如下图所示:

(1)为确保实验的准确性,要先检查装置的 ;
(2)实验开始,先用弹簧夹夹紧乳胶管,再将注射器内等体积的水和NaOH溶液分别注入充满SO2的集气瓶;
(3)充分吸收SO2后,打开弹簧夹,观察实验后进入两个集气瓶内植物油的体积.
【结论与解释】
(1)甲实验中,SO2溶于水且与水反应生成H2SO3,反应的化学方程式为 ;
(2)乙实验中,SO2与NaoH发生反应最终生成NaHSO3;
(3)分析实验现象得知,用碱性溶液比用水吸收SO2的效果 .
【拓展与迁移】
(1)在必须用煤作燃料的情况下.要减少SO2的排放,请你提出一条合理化建议:.
【提出问题】SO2是形成酸雨的主要物质.由此想到,选用氢氧化钠等碱性溶液吸收SO2,效果会怎样?
【设计与实验】用两套完全相同的装置做对比实验(SO2不溶于植物油也不与其反应),如下图所示:

(1)为确保实验的准确性,要先检查装置的
(2)实验开始,先用弹簧夹夹紧乳胶管,再将注射器内等体积的水和NaOH溶液分别注入充满SO2的集气瓶;
(3)充分吸收SO2后,打开弹簧夹,观察实验后进入两个集气瓶内植物油的体积.
【结论与解释】
(1)甲实验中,SO2溶于水且与水反应生成H2SO3,反应的化学方程式为
(2)乙实验中,SO2与NaoH发生反应最终生成NaHSO3;
(3)分析实验现象得知,用碱性溶液比用水吸收SO2的效果
【拓展与迁移】
(1)在必须用煤作燃料的情况下.要减少SO2的排放,请你提出一条合理化建议:.
考点:酸雨的产生、危害及防治,碱的化学性质,书写化学方程式、文字表达式、电离方程式
专题:化学与环境保护
分析:主要是利用瓶内压强的变化来证明二氧化硫和水及氢氧化钠溶液反应程度的不同,进入的水越多,说明瓶内压强减少的越多,即瓶内气体被吸收的越多.
解答:解:
【设计与实验】
(1)由于装置的气密性影响实验的成败,因此在实验前必须要验证装置的气密性,故答案为:气密性
【结论与解释】
①由于二氧化硫和水反应生成亚硫酸,故答案为:SO2+H2O=H2SO3
③由于乙实验中集气瓶中进入的水远远大于甲实验中集气瓶进入的水,因此氢氧化钠溶液吸收二氧化硫更彻底,故答案为:好一些
[拓展与迁移]由于二氧化硫是一种有毒的气体,排放到空气中会污染空气,为减少二氧化硫的排放,可以使用含有生石灰或石灰石的煤,脱硫,或使用优质煤,故答案为:使用优质煤(或使用脱硫煤)
答案:
【设计与实验】(1)检查装置的气密性;
【结论与解释】(1)SO2+H2O═H2SO3; (3)好一些.
【拓展与迁移】(1)使用优质煤(或使用含硫量低的煤,使用脱硫煤)
【设计与实验】
(1)由于装置的气密性影响实验的成败,因此在实验前必须要验证装置的气密性,故答案为:气密性
【结论与解释】
①由于二氧化硫和水反应生成亚硫酸,故答案为:SO2+H2O=H2SO3
③由于乙实验中集气瓶中进入的水远远大于甲实验中集气瓶进入的水,因此氢氧化钠溶液吸收二氧化硫更彻底,故答案为:好一些
[拓展与迁移]由于二氧化硫是一种有毒的气体,排放到空气中会污染空气,为减少二氧化硫的排放,可以使用含有生石灰或石灰石的煤,脱硫,或使用优质煤,故答案为:使用优质煤(或使用脱硫煤)
答案:
【设计与实验】(1)检查装置的气密性;
【结论与解释】(1)SO2+H2O═H2SO3; (3)好一些.
【拓展与迁移】(1)使用优质煤(或使用含硫量低的煤,使用脱硫煤)
点评:主要考查了二氧化硫的有关的化学性质,能用所学的知识来解释所看到的现象,培养学生的分析能力和解决问题的能力.

练习册系列答案
相关题目
下列有关托盘天平的使用,操作错误的是( )
| A、称量前要检查天平是否平衡 |
| B、称量时把称量物放在右盘,砝码放左盘 |
| C、取用砝码要用镊子,添加顺序一般由大到小 |
| D、称量完毕后,应把砝码放回砝码盒中,把游码移回零处 |
把一瓶稀盐酸平均分成两份装在甲、乙两个烧杯中,把等质量的碳酸镁和碳酸钠粉末分别放入甲、乙两个烧杯中,下列分析结论正确的是( )
| A、反应后碳酸镁有剩余甲烧杯产生的气体一定多 |
| B、反应后发现碳酸钠剩余乙烧杯产生的气体多 |
| C、反应后碳酸钠剩余,甲、乙两个烧杯中产生的气体一样多 |
| D、反应后碳酸钠全部消失,甲、乙两个烧杯中产生的气体可能一样多 |
 从分子的角度分析并解释下列问题.
从分子的角度分析并解释下列问题.