题目内容
向10g质量分数为2%的NaOH溶液中逐滴加入10g质量分数为2%的盐酸,反应过程中,溶液的pH随加入盐酸的质量(m)的变化而发生变化,下列图象中能正确反映这种情况的是( )
A、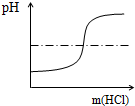 |
B、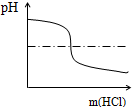 |
C、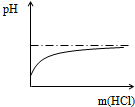 |
D、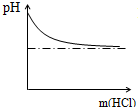 |
考点:中和反应及其应用,溶液的酸碱性与pH值的关系,根据化学反应方程式的计算
专题:常见的酸 酸的通性
分析:氢氧化钠溶液和盐酸反应生成氯化钠和水,氢氧化钠的PH大于7,盐酸PH小于7,根据溶液的PH与加入的盐酸的量的关系分析.
解答:解:
A、氢氧化钠溶液的PH大于7,图象中开始时溶液的PH小于7.故错误;
B、根据NaOH+HCl═NaCl+H2O 10g质量分数为2%的NaOH溶液中NaOH的质量为0.2g,10g质量分数为2%的盐酸中氯化氢的直来那个为10g×2%=0.2g
40 36.5
0.2g 0.2g
由此看出,盐酸过量,溶液的PH小于7,故正确;
C、氢氧化钠溶液的PH大于7,图象中开始时溶液的PH小于7.故错误;
D、向氢氧化钠溶液中逐滴加入盐酸,当盐酸过量时,溶液的PH小于7.故错误.
答案:B.
A、氢氧化钠溶液的PH大于7,图象中开始时溶液的PH小于7.故错误;
B、根据NaOH+HCl═NaCl+H2O 10g质量分数为2%的NaOH溶液中NaOH的质量为0.2g,10g质量分数为2%的盐酸中氯化氢的直来那个为10g×2%=0.2g
40 36.5
0.2g 0.2g
由此看出,盐酸过量,溶液的PH小于7,故正确;
C、氢氧化钠溶液的PH大于7,图象中开始时溶液的PH小于7.故错误;
D、向氢氧化钠溶液中逐滴加入盐酸,当盐酸过量时,溶液的PH小于7.故错误.
答案:B.
点评:本题是化学反应中定量关系和图象相结合的题型,题目难度较大.要准确解答此类题,关键要对化学反应知识熟练,并能结合图象的数学意义,综合考虑,可快速解答.图象的意义要抓住三点:①抓图象的起点,②抓图象的终点,③抓图象的变化过程.具体可结合解答领会.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列过程只体现了物质物理性质的是( )
| A、用铜丝做导线 |
| B、氧气用于火箭发射 |
| C、用稀盐酸除水垢 |
| D、液化石油气用作燃料 |
薯片等极易碎食品宜采用充气包装,下列气体中最不适宜充入的是( )
| A、O2 |
| B、N2 |
| C、CO2 |
| D、He |
下列物质中含有氧气的是( )
| A、双氧水 | B、空气 |
| C、氯酸钾 | D、二氧化锰 |
目前还没有被列入我国城市空气质量监测项目的物质是( )
| A、二氧化硫 | B、二氧化氮 |
| C、二氧化碳 | D、可吸入颗粒物 |
 如图所示实验装置可用于测定空气中氧气的含量,实验前在集气瓶中加入少量的水,将瓶内剩余部分分为五等份,并做上标记.实验过程如下:
如图所示实验装置可用于测定空气中氧气的含量,实验前在集气瓶中加入少量的水,将瓶内剩余部分分为五等份,并做上标记.实验过程如下:
