题目内容
19.如图是配制溶质质量分数为10%的NaCl溶液的实验操作示意图.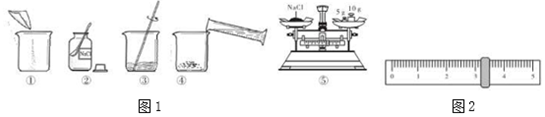
(1)用如图1的序号表示配制溶液的正确操作顺序②⑤①④③;
(2)图②中,有一种取药品的仪器,其名称是药匙,图③中玻璃棒的作用搅拌,加快溶解速率;
(3)称量NaCl时,天平平衡后的装置如图⑤所示,游码标尺示数如图2,则称取的NaCl质量为18.2g,根据计算需要量取水的体积是163.8mL(水的密度为1g/ml);
(4)称量NaCl质量完毕放回砝码时,发现有一个砝码缺损了一个小角,若其他操作步骤正确,则所配溶液的溶质质量分数小于10%(填“大于”“小于”或“等于”).
分析 (1)根据配制溶质质量分数一定的溶液的基本步骤,进行分析解答.
(2)根据常见仪器的名称、操作③是溶解操作,进行分析解答.
(3)根据托盘天平的使用方法,利用溶液质量=溶质质量÷溶质的质量分数,溶剂质量=溶液质量-溶质质量即可求得水的质量.结合量筒的使用方法,进行分析解答.
(4)砝码缺少一角,则称量的NaCl的质量减小,可以据此进一步分析对所配溶液的溶质质量分数的影响情况.
解答 解:(1)配制溶质质量分数为10%的NaCl溶液,首先计算配制溶液所需氯化钠和水的质量,再称量所需的氯化钠和量取水,最后进行溶解,故正确顺序是②⑤①④③.
(2)图②中,有一种取药品的仪器,其名称是药匙;操作③是溶解操作,玻璃棒的作用是搅拌,加快溶解速率.
(3)称量NaCl时,天平平衡后的状态如图⑤所示,游码标尺示数如图2,则称取的NaCl质量为10g+5g+3.2g=18.2g.
溶液质量=溶质质量÷溶质的质量分数,配制溶质质量分数为10%的NaCl溶液的质量为18.2g÷10%=182g;溶剂质量=溶液质量-溶质质量,则所需水的质量=182g-18.2g=163.8g(合163.8mL).
(4)NaCl的质量=砝码的质量+游码的质量,据图可知,砝码的读数是10g+5g=15g,游码的读数是3.2g,但砝码缺少一角,说明砝码的质量小于15g,则称量的NaCl的质量小于15g,则溶质质量偏少,溶剂的质量不变,则导致所配制的溶质质量分数偏小.
故答案为:(1)②⑤①④③;(2)药匙;搅拌,加快溶解速率;(3)18.2g;163.8mL;(4)小于.
点评 本题难度不大,明确配制一定溶质质量分数的溶液实验步骤(计算、称量、溶解)、注意事项等是正确解答本题的关键.

练习册系列答案
相关题目
14.请将有关物质俗称或化学式填在下表空格内:
| 物质俗称 | 甲烷 | 大理石或石灰石 | 铁锈 | 熟石灰或消石灰 |
| 化学式 | CH4 | CaCO3 | Fe2O3 | Ca(OH)2 |
9.对“10%的食盐溶液”含义的解释错误的是( )
| A. | 100 g水中溶解了10 g食盐 | |
| B. | 100 g食盐溶液溶解有10 g食盐 | |
| C. | 将10 g食盐溶解于90 g水中所得的溶液 | |
| D. | 将食盐与水按1:9的质量比配成的溶液 |
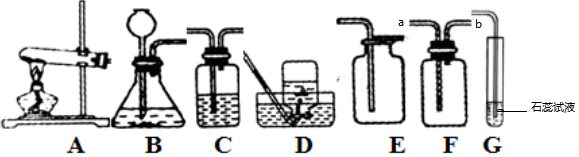

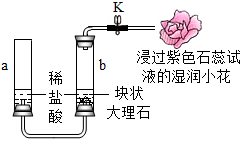 王杰同学学习了二氧化碳的制取和性质知识后,利用家庭物品设计实验研究二氧化碳的性质.
王杰同学学习了二氧化碳的制取和性质知识后,利用家庭物品设计实验研究二氧化碳的性质.