题目内容
7.水和溶液在生产生活中起着重要的作用.(1)电解水实验可以得出水的组成,该反应的化学方程式为2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.
(2)过滤是净化水的方法之一.在实验室进行过滤操作时应注意做到
“一贴、二低、三靠”,其中的“二低”是指滤纸边缘低于漏斗边缘、液面低于滤纸边缘.
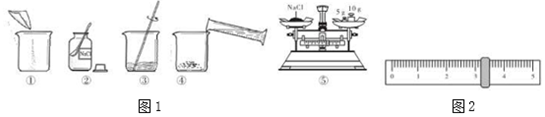
(3)现将300g 25%的NaCl溶液稀释为10%的NaCl溶液,需要加水的质量为450g;配制的主要步骤有:计算、称量、混匀、装瓶并贴上标签;实验中用到的玻璃仪器是烧杯、量筒、玻璃棒和试剂瓶.
(4)①甲、乙两物质的溶解度曲线如图1所示.20℃时,将等质量的甲、乙两种固体,分别加入盛有10g水的A、B试管中,充分溶解后,可观察到如图2所示的现象.则20℃<t℃(填“>”、“<”或“=”).

②20℃时,对A试管进行如下操作,最终A试管中溶液溶质的质量分数一定发生变化的是C(填字母序号).
A.加少量水 B.加入少量甲物质
C.升温到40℃D.蒸发部分溶剂,恢复到20℃
分析 (1)电解水生成氢气和氧气;
(2)“一贴、二低、三靠”,其中的“二低”是指滤纸边缘低于漏斗边缘、液面低于滤纸边缘;
(3)溶液稀释前后,溶质质量不变;
(4)根据物质的溶解度曲线及其提供的数据可以判断相关方面的问题.
解答 解:(1)电解水实验可以得出水的组成,该反应的化学方程式为:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.
故填:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.
(2)“一贴、二低、三靠”,其中的“二低”是指滤纸边缘低于漏斗边缘、液面低于滤纸边缘.
故填:滤纸边缘低于漏斗边缘;液面低于滤纸边缘.
(3)将300g 25%的NaCl溶液稀释为10%的NaCl溶液,需要加水的质量为:300g×25%÷10%-300g=450g;
配制的主要步骤有:计算、称量、混匀、装瓶并贴上标签;
实验中用到的玻璃仪器是烧杯、量筒、玻璃棒和试剂瓶.
故填:450;称量;烧杯、量筒、玻璃棒.
(4)①A中固体没有完全溶解,B中固体完全溶解,说明乙的溶解度比甲的溶解度大,由溶解度曲线可知,温度小于t℃时乙的溶解度大于甲,因此20℃<t℃,
故填:<.
②A.加少量水时,固体继续溶解,如果没有完全溶解或恰好完全溶解,溶质质量分数不变;
B.加入少量甲物质时,不能继续溶解,溶质质量分数不变;
C.升温到40℃时,由于甲的溶解度随着温度升高而增大,因此固体继续溶解,溶质质量分数增大;
D.蒸发部分溶剂,恢复到20℃时,仍然是饱和溶液,溶质质量分数不变.
故填:C.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

 一线名师权威作业本系列答案
一线名师权威作业本系列答案| A. | 氢氧化钠 | B. | 熟石灰 | C. | 果酸 | D. | 氢氧化铝 |
| A. | 瓶口有气泡冒出 | B. | 带火星的木条伸入集气瓶中 | ||
| C. | 燃烧的木条伸入集气瓶中 | D. | 带火星的木条放在集气瓶口 |