题目内容
17.霸树化学小组用一定量AgNO3和Al(NO3)3的混合溶液加入铜粉和锌粉,充分反应后过滤,得到滤液和滤渣.则①滤液中一定含有Al(NO3)3和Zn(NO3)2;②滤渣中一定含有Ag,可能含有Cu和Zn;③若滤液显蓝色,则滤液中一定含有Al(NO3)3、Zn(NO3)2和Cu(NO3)2;④若向滤渣滴加稀盐酸有气泡产生,则滤液中一定没有AgNO3和Cu(NO3)2.以上说法正确的是( )| A. | ①② | B. | ②③④ | C. | ①③④ | D. | ①②③④ |
分析 在金属活动性顺序中,排在前面的金属可以把位于它后面的金属从其盐溶液中置换出来,可简记为“前置后,盐可溶”.
解答 解:在金属活动顺序表中,由于金属的活动性顺序是:铝>锌>铜>银,向一定量AgNO3和Al(NO3)3的混合溶液加入铜粉和和锌粉,锌先与AgNO3反应生成了硝酸锌和银,不能与Al(NO3)3反应,当锌完全反应后,铜再与AgNO3反应生成了硝酸铜和银.由此可知:
①滤液中一定含有Al(NO3)3和Zn(NO3)2,故正确;
②滤渣中一定含有Ag,可能含有Cu和Zn,故正确;
③若滤液显蓝色,说明了锌完全反应了,铜也参加了反应,则滤液中一定含有Al(NO3)3、Zn(NO3)2和Cu(NO3)2,故正确;
④若向滤渣滴加稀盐酸有气泡产生,说明了锌有剩余,滤液中一定没有AgNO3和Cu(NO3)2,故正确.
由以上分析可知D正确.
故答案选D.
点评 本题考查了金属活动性顺序的应用,完成此题,可以依据金属活动性顺序及其意义进行.

练习册系列答案
相关题目
12.填写实验报告:
| 实验内容 | 实验现象 | 分析与判断 |
| 1盐和金属的反应 取一支洁净的试管,向试管中加入3ml的硫酸铜溶液,小心地加入一根用砂纸打磨光亮的铁丝,静置 | 铁丝表面生成红色固体,溶液由蓝色变浅绿色 | 化学方程式Fe+CuSO4=FeSO4+Cu |
| 2盐和碱的反应 取一支洁净的试管,向试管中加入约2ml碳酸钠溶液,用滴管向碳酸钠溶液中逐滴滴加氢氧化钙或氢氧化钡溶液,观察 | 生成白色沉淀 | 原因是生成的CaCO3或BaCO3(填化学式)难溶于水 |
6.下列图象不能正确反映其变化过程的是( )
| A. |  镁在装有空气的密闭容器内燃烧 | |
| B. |  电解水生成气体的体积 | |
| C. |  浓硫酸长期露置在空气中 | |
| D. |  向空气中部分变质的氢氧化钠溶液中滴加稀盐酸 |
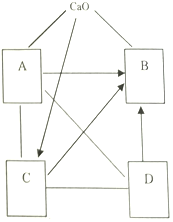 如图中A、B、C、D分别表示初中常见不同类别的四种物质,A由两种元素组成,图中用“-”表示两种物质之间能发生化学反应,用“→”表示一种物质可以转化为另一种物质,部分反应物和生成物及反应条件已略去,(图中部分反应需在溶液中进行),请回答下列问题
如图中A、B、C、D分别表示初中常见不同类别的四种物质,A由两种元素组成,图中用“-”表示两种物质之间能发生化学反应,用“→”表示一种物质可以转化为另一种物质,部分反应物和生成物及反应条件已略去,(图中部分反应需在溶液中进行),请回答下列问题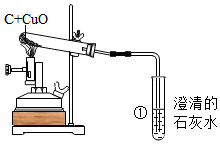 某同学为了探究木炭和氧化铜在高温条件下生成的气体产物的成分,提出了如下猜想:
某同学为了探究木炭和氧化铜在高温条件下生成的气体产物的成分,提出了如下猜想: