题目内容
4. 奥运会“祥云”火炬载着中国人民对世界人民的友谊,在全球传递.它采用的燃料是丙烷(分子结构模型如图所示),下列关于丙烷分子的说法不正确的是( )
奥运会“祥云”火炬载着中国人民对世界人民的友谊,在全球传递.它采用的燃料是丙烷(分子结构模型如图所示),下列关于丙烷分子的说法不正确的是( )| A. | 丙烷属于有机物 | |
| B. | 丙烷的化学式可表示为C3H8 | |
| C. | 丙烷分子中碳原子和氢原子的个数比为3:8 | |
| D. | 丙烷中碳、氢元素的质里比是3:8 |
分析 A.根据有机物的概念来分析;
B.根据微观结构示意图来分析;
C.根据分子结构来分析;
D.根据化合物中元素的质量比来分析.
解答 解:根据丙烷分子模型,可看出每个丙烷分子由3个碳原子、8个氢原子构成,化学式为C3H8.
A.丙烷是一种含碳元素的化合物,属于有机物,故正确;
B.根据丙烷分子模型,可看出每个丙烷分子由3个碳原子、8个氢原子构成,化学式为C3H8.故正确;
C.根据丙烷分子模型,可看出每个丙烷分子由3个碳原子、8个氢原子构成,因此丙烷分子中碳原子和氢原子的个数比为3:8;故正确;
D.根据丙烷分子模型,可看出每个丙烷分子由3个碳原子、8个氢原子构成,碳元素和氢元素的质量比为(12×3):(1×8)=9:2;故不正确.
故选D.
点评 根据物质的分子结构模型可以直观地看出构成物质的分子的构成,依据分子的构成可推断物质的组成等.

练习册系列答案
 提分百分百检测卷系列答案
提分百分百检测卷系列答案
相关题目
15.有一包白色粉末,可能含有氯化钡、氢氧化钠、碳酸氢铵、氯化钠、无水硫酸铜、碳酸钙中的一种或几种.为确定其组成,进行如下实验:
①取少量该粉末置于烧杯中,未嗅到任何气味;向烧杯中加入适量的水,充分搅拌,静置后,观察到上层溶液呈无色,烧杯底部有蓝白色固体;过滤.
②向上述滤液中滴加几滴硝酸银溶液,溶液变浑浊.
③将上述滤渣投入盛有足量稀盐酸的烧杯中,充分搅拌,有无色无味的气体产生,烧杯底部有白色固体剩余.
则下列说法正确的是( )
①取少量该粉末置于烧杯中,未嗅到任何气味;向烧杯中加入适量的水,充分搅拌,静置后,观察到上层溶液呈无色,烧杯底部有蓝白色固体;过滤.
②向上述滤液中滴加几滴硝酸银溶液,溶液变浑浊.
③将上述滤渣投入盛有足量稀盐酸的烧杯中,充分搅拌,有无色无味的气体产生,烧杯底部有白色固体剩余.
则下列说法正确的是( )
| A. | 白色粉末中可能有氯化钠和碳酸钙 | |
| B. | 白色粉末中肯定没有氢氧化钠和碳酸氢铵,可能有氯化钠 | |
| C. | 白色粉末中肯定有氯化钡、氢氧化钠、无水硫酸铜和碳酸钙 | |
| D. | 白色粉末中肯定有氢氧化钠和无水硫酸铜,且二者的质量比一定为1﹕2 |
12.下列实验设计能达到实验目的是C.
| 实验目的 | 实验设计 | |
| A | 除去CO中的少量H2O和CO2 | 先通过浓硫酸,再通过氢氧化钠溶液 |
| B | 除去NaCl固体中的少Ma2CO3 | 先加足量水溶解,再加适稀硫酸,蒸发 |
| C | 除去KN03,溶液中的少量K2SO4 | 加入适量的Ba(N03)2溶液,过滤 |
| D | 除去铜粉中混有的少量铁粉 | 用磁铁吸引 |
19.科学兴趣小组的同学在老师的指导下,对用铁碳合金制作的井盖中单质铁的含量进行了测定.他们请老师将一块破碎的井盖样品进行粉碎处理,四组同学各取12.0g 粉末样品罝于烧杯中,然后加入一定质量的稀硫酸,充分反应后,对烧杯中剩余固体进行称量,相关的实验数据记录如表:
(1)分析上表数据可知,编号为3组的同学其剩余固体质量的数据不合理.
(2)该井盖样品中单质铁的质量分数=93.3%(结果保留至0.1%)
(3)反应所用硫酸溶液中溶质的质量分数是多少?(写出计算过程)
(4)如果井盖已生锈,你认为要准确地测得样品中铁元素的质量分数,应该将上述实验中测量“剩余固体质量”改成测量下列中的C(填字母).
A.加入稀硫酸的体积
B.反应完全后烧杯中所有物质的质量
C.反应完全后烧杯中所有物质的质量和剩余固体质量.
| 组别 编号 | 样品质量/g | 加入稀硫酸质量/g | 剩余固体 质量/g |
| 1 | 12.0 | 80.0 | 0.8 |
| 2 | 12.0 | 80.0 | 0.8 |
| 3 | 12.0 | 100.0 | 1.0 |
| 4 | 12.0 | 100.0 | 0.8 |
(2)该井盖样品中单质铁的质量分数=93.3%(结果保留至0.1%)
(3)反应所用硫酸溶液中溶质的质量分数是多少?(写出计算过程)
(4)如果井盖已生锈,你认为要准确地测得样品中铁元素的质量分数,应该将上述实验中测量“剩余固体质量”改成测量下列中的C(填字母).
A.加入稀硫酸的体积
B.反应完全后烧杯中所有物质的质量
C.反应完全后烧杯中所有物质的质量和剩余固体质量.
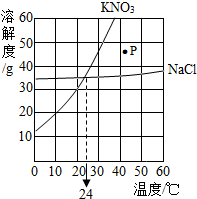 图为硝酸钾和氯化钠的溶解度曲线.由图可知:
图为硝酸钾和氯化钠的溶解度曲线.由图可知: