题目内容
某化合物A在氧气中充分燃烧后只生成二氧化碳和水,为确定A的组成,某同学进行了如下探究.
【猜想】猜想一:A中只含C、H两种元素 猜想二:A中含C、H、O三种元素
【实验】
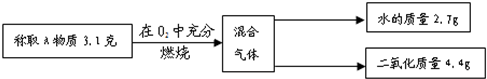
(1)根据 判断A中一定含 .
(2)参加反应的O2的质量为: ,混合气体中的氧元素的质量为: .则可判断 正确.
(3)还可根据 判断猜想二正确.
【猜想】猜想一:A中只含C、H两种元素 猜想二:A中含C、H、O三种元素
【实验】

(1)根据
(2)参加反应的O2的质量为:
(3)还可根据
考点:质量守恒定律及其应用,化合物中某元素的质量计算
专题:化学用语和质量守恒定律
分析:化学反应遵循质量守恒定律,即化学反应前后,元素的种类不变,原子的种类、总个数不变.
解答:解:(1)根据质量守恒定律可知,A中一定含碳元素和氢元素.
故填:碳元素和氢元素.
(2)参加反应的O2的质量为:2.7g+4.4g-3.1g=4g;
混合气体中的氧元素的质量为:2.7g×
×100%+4.4g×
×100%=5.6g;
则A物质中氧元素的质量为:5.6g-4g=1.6g,
则可判断猜想二正确.
故填:4g;5.6g;猜想二.
(3)如果A的质量大于水、二氧化碳中的C、H元素的质量和,则A中含有氧元素;如果A的质量等于水、二氧化碳中的C、H元素的质量和,则A中不含有氧元素.
故填:比较A的质量和水、二氧化碳中的C、H元素的质量和.
故填:碳元素和氢元素.
(2)参加反应的O2的质量为:2.7g+4.4g-3.1g=4g;
混合气体中的氧元素的质量为:2.7g×
| 16 |
| 18 |
| 32 |
| 44 |
则A物质中氧元素的质量为:5.6g-4g=1.6g,
则可判断猜想二正确.
故填:4g;5.6g;猜想二.
(3)如果A的质量大于水、二氧化碳中的C、H元素的质量和,则A中含有氧元素;如果A的质量等于水、二氧化碳中的C、H元素的质量和,则A中不含有氧元素.
故填:比较A的质量和水、二氧化碳中的C、H元素的质量和.
点评:化学反应遵循质量守恒定律,即化学反应前后,元素的种类不变,原子的种类、总个数不变,这是书写化学方程式、进行相关方面计算的基础.

练习册系列答案
 同步练习强化拓展系列答案
同步练习强化拓展系列答案
相关题目
下列各组括号内除杂质的方法或试剂错误的是( )
| A、Cu粉中混有铁粉(硫酸铜溶液) |
| B、硝酸钠溶液中混有NaCl(AgNO3溶液) |
| C、C粉中混有CuO(稀硫酸) |
| D、CaO中混有CaCO3(稀盐酸) |
 电解水的实验装置如图所示,根据图回答:
电解水的实验装置如图所示,根据图回答: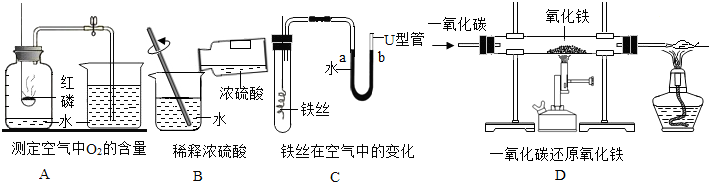
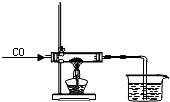 如图进行实验,如果硬质试管中的药品是CuO,实验现象为
如图进行实验,如果硬质试管中的药品是CuO,实验现象为