题目内容
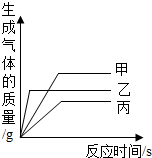 等质量的甲、乙、丙三种金属的粉末,与足量的稀硫酸反应(反应后甲、乙、丙三种金属都显+2价),生成H2的质量与反应时间的关系如图所示,下列说法错误的是( )
等质量的甲、乙、丙三种金属的粉末,与足量的稀硫酸反应(反应后甲、乙、丙三种金属都显+2价),生成H2的质量与反应时间的关系如图所示,下列说法错误的是( )| A、三种金属的活泼性:乙>甲>丙 |
| B、生成氢气的质量:甲>乙>丙 |
| C、相对原子质量:甲>乙>丙 |
| D、消耗硫酸的质量:甲>乙>丙 |
考点:金属的化学性质
专题:金属与金属材料
分析:A、根据相同时间内产生氢气较多(即反应剧烈)的金属活动性较强,结合产生氢气的关系图判断三种金属活动性;
B、根据图象分析生成氢气的质量;
C、根据甲、乙、丙在生成物中化合价均为+2价可知一定质量的金属完全反应产生氢气的质量与金属的相对原子质量成反比分析;
D、根据质量守恒定律定律可知,生成氢气的质量取决于消耗的硫酸的质量.
B、根据图象分析生成氢气的质量;
C、根据甲、乙、丙在生成物中化合价均为+2价可知一定质量的金属完全反应产生氢气的质量与金属的相对原子质量成反比分析;
D、根据质量守恒定律定律可知,生成氢气的质量取决于消耗的硫酸的质量.
解答:解:A、根据反应生成H2的质量与反应时间的关系图所示,当三种金属都在发生反应时,相同时间内乙放出氢气的质量大于甲、大于丙,可判断三种金属活动性顺序是乙>甲>丙,故说法正确;
B、根据反应生成H2的质量与反应时间的关系图所示,在三种金属完全反应后,放出H2的质量是甲>乙>丙,故说法正确;
C、三种金属的化合价、金属的质量都相等,完全反应放出氢气的质量与金属的相对原子质量成反比,即产生氢气多的相对原子质量小;根据反应生成H2的质量与反应时间的关系图所示,在三种金属完全反应后,放出H2的质量是甲>乙>丙,因此可判断相对原子质量是丙>乙>甲,故说法错误;
D、金属与酸的反应生成氢气时,氢气来源于酸中的氢元素,所以生成的氢气与消耗的酸的多少顺序一致,消耗硫酸的质量:甲>乙>丙,故说法正确.
故选C.
B、根据反应生成H2的质量与反应时间的关系图所示,在三种金属完全反应后,放出H2的质量是甲>乙>丙,故说法正确;
C、三种金属的化合价、金属的质量都相等,完全反应放出氢气的质量与金属的相对原子质量成反比,即产生氢气多的相对原子质量小;根据反应生成H2的质量与反应时间的关系图所示,在三种金属完全反应后,放出H2的质量是甲>乙>丙,因此可判断相对原子质量是丙>乙>甲,故说法错误;
D、金属与酸的反应生成氢气时,氢气来源于酸中的氢元素,所以生成的氢气与消耗的酸的多少顺序一致,消耗硫酸的质量:甲>乙>丙,故说法正确.
故选C.
点评:对于活泼金属,活动性越强的金属与酸反应越剧烈,即反应放出氢气的速度越快;化合价相同的等质量金属完全反应放出氢气的质量与金属的相对原子质量成反比.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
实验室中装有红磷的试剂瓶上应贴有的图标是( )
A、 |
B、 |
C、 |
D、 |
下列是一些粒子的结构示意图,有关说法错误的是( 

| A、③⑤属于同种元素的不同种粒子 |
| B、①表示的是阳离子,③表示的是阴离子 |
| C、②④两种元素的化学性质相似 |
| D、②④属于元素周期表中不同纵行的原子 |
检验集气瓶中是否收集满二氧化碳可采用的方法是( )
| A、倒入澄清的石灰水并振荡 |
| B、用燃着的木条伸入集气瓶的下部 |
| C、用燃着木条伸入集气瓶口观察 |
| D、捉一小虫放入集气瓶中观察 |

