题目内容
为探究镁、铝、铜、银的金属活动性顺序,化学兴趣小组设计了如图三个实验(所有金属均已打磨,其形状、大小相同,所有稀硫酸的溶质质量分数及体积相同):

(1)小组同学认为,通过实验①和②可以比较镁和铝的金属活动性,他们依据的实验现象是 .
(2)一段时间后,取出实验③中的铜片,观察到其表面有银白色物质,说明铜的活动性比银强,该反应的化学方程式是 ;
(3)小组中有同学认为,上述实验方案不足以得出四种金属的活动性顺序,她在上述实验的基础上,用一种金属和一种盐溶液反应,实现了探究目的.她所用的金属是 ,盐溶液是 溶液.

(1)小组同学认为,通过实验①和②可以比较镁和铝的金属活动性,他们依据的实验现象是
(2)一段时间后,取出实验③中的铜片,观察到其表面有银白色物质,说明铜的活动性比银强,该反应的化学方程式是
(3)小组中有同学认为,上述实验方案不足以得出四种金属的活动性顺序,她在上述实验的基础上,用一种金属和一种盐溶液反应,实现了探究目的.她所用的金属是
考点:金属活动性顺序及其应用,书写化学方程式、文字表达式、电离方程式
专题:金属与金属材料
分析:根据金属与酸反应产生气泡的速率可以判断金属的活动性强弱,在金属活动性顺序中,位置在前的金属能将位于其后的金属从其盐溶液中置换出来.据此分析有关的问题.
解答:解:(1)由于金属与酸反应产生气泡的速率可以判断金属的活动性强弱,所以,通过实验①和②可以比较镁和铝的金属活动性,依据的实验现象是:①中试管产生气泡的速度快.
(2)一段时间后,取出实验Ⅲ中的铜片,观察到其表面有银白色物质,说明铜能将银从其溶液中置换出来,铜比银活泼,反应的化学方程式是:Cu+2AgNO3═Cu(NO3)2+2Ag.
(3)通过上述实验,能比较出镁比铝活泼,铜比银活泼,但不能比较铝与铜的活泼关系,则补充实验是铝片和硫酸铜溶液的反应,达到实验目的.所以,她所用的金属是铝,盐溶液是硫酸铜溶液.
故答为:(1)①中试管产生气泡的速度快;(2)Cu+2AgNO3═Cu(NO3)2+2Ag;(3)铝;硫酸铜.
(2)一段时间后,取出实验Ⅲ中的铜片,观察到其表面有银白色物质,说明铜能将银从其溶液中置换出来,铜比银活泼,反应的化学方程式是:Cu+2AgNO3═Cu(NO3)2+2Ag.
(3)通过上述实验,能比较出镁比铝活泼,铜比银活泼,但不能比较铝与铜的活泼关系,则补充实验是铝片和硫酸铜溶液的反应,达到实验目的.所以,她所用的金属是铝,盐溶液是硫酸铜溶液.
故答为:(1)①中试管产生气泡的速度快;(2)Cu+2AgNO3═Cu(NO3)2+2Ag;(3)铝;硫酸铜.
点评:金属活动性顺序的应用主要表现在两个方面:一是只有排在氢前面的金属才能与酸反应,生成氢气和盐(位置越靠前,反应越剧烈),二是金属与盐溶液的反应时,只有排在前面的金属才能将排在它后面的金属从它的盐溶液中置换出来.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
由质量守恒定律可知,化学反应前后,一定不变的是( )
①原子种类 ②原子数 ③分子种类 ④分子数目 ⑤元素种类 ⑥物质种类.
①原子种类 ②原子数 ③分子种类 ④分子数目 ⑤元素种类 ⑥物质种类.
| A、①②③④⑤⑥ | B、④⑤⑥ |
| C、①②⑤ | D、③④⑤ |
下列化学符号正确的是( )
| A、1个一氧化碳分子:Co |
| B、2个氢原子:H2 |
| C、铁元素的化合价为+3价:Fe+3 |
| D、2个碳酸根离子:2CO32- |
小宇同学在化学课上提出,可用磁铁来检验某种金属是否是铁,就这一过程而言,属于科学探究环节中的( )
| A、交流评价 | B、获得结论 |
| C、设计实验 | D、提出问题 |
我国著名化工专家侯德榜作出的重大贡献是( )
| A、发明黑火药 |
| B、创造湿法冶金 |
| C、改进了纯碱的生产工艺 |
| D、发现了新元素 |
市场上某补钙制剂的说明书如图所示:则每天需补充的钙为( )

| A、0.25 g |
| B、0.5 g |
| C、0.625 g |
| D、1.2 5g |
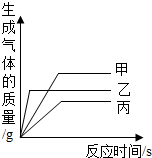 等质量的甲、乙、丙三种金属的粉末,与足量的稀硫酸反应(反应后甲、乙、丙三种金属都显+2价),生成H2的质量与反应时间的关系如图所示,下列说法错误的是( )
等质量的甲、乙、丙三种金属的粉末,与足量的稀硫酸反应(反应后甲、乙、丙三种金属都显+2价),生成H2的质量与反应时间的关系如图所示,下列说法错误的是( )| A、三种金属的活泼性:乙>甲>丙 |
| B、生成氢气的质量:甲>乙>丙 |
| C、相对原子质量:甲>乙>丙 |
| D、消耗硫酸的质量:甲>乙>丙 |

