题目内容
有铁粉和铜粉的均匀混合物,甲、乙、丙三位同学分别取该混合物与稀硫酸反应,所得数据如表所示:
|
|
甲 |
乙 |
丙 |
|
金属混合物质量/g |
10 |
10 |
20 |
|
稀硫酸质量/g |
100 |
120 |
100 |
|
剩余固体质量/g |
4 |
4 |
13 |
请分析数据,回答下列问题:
(1)甲同学所得溶液中含有的溶质是 .
(2)计算丙同学所得溶液中溶质的质量分数.(计算结果精确到0.1%)
(1)H2SO4、FeSO4;(2)17.8%.
【解析】
试题分析:(1)根据金属的活动性关系铁>氢>铜,铁能与稀硫酸反应生成硫酸亚铁同时放出氢气,而铜不能与稀硫酸反应,当把金属混合物放入足量稀硫酸中充分反应时,剩余固体为铜,而金属混合物中铁的质量为混合物质量与铜质量差.由丙可知100g硫酸能与7g铁粉反应,所以甲中只与6g铁反应,说明硫酸过量,所以反应后溶质是硫酸亚铁和硫酸化学式是:H2SO4、FeSO4
(2)解:参加反应的铁的质量为:20g﹣13g=7g.
设生成硫酸亚铁的质量为x,生成氢气的质量为y
Fe+H2SO4=FeSO4+H2↑
56 152 2
7g x y
根据: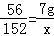 解得 x=19g,根据:
解得 x=19g,根据: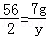 解得 y=0.25 g
解得 y=0.25 g
所以反应后溶液质量为:20g﹣13g+100g﹣0.25g=106.75 g
反应后溶液中硫酸亚铁的质量分数为: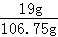 ×100%≈17.8%
×100%≈17.8%
答:丙同学所得溶液中硫酸亚铁的质量分数为17.8%
考点:根据化学反应方程式的计算;有关溶质质量分数的简单计算.

 一本好题口算题卡系列答案
一本好题口算题卡系列答案有铁粉和铜粉的均匀混合物,甲、乙、丙三位同学分别取该混合物与稀硫酸反应,所得数据如下表所示:
| 甲 | 乙 | 丙 | |
| 取用金属混合物的质量/g | 10 | 10 | 20 |
| 取用稀硫酸的质量/g | 100 | 120 | 100 |
| 反应后过滤,得干燥固体的质量/g | 4 | 4 | 13 |
请分析数据,回答下列问题:
(1)甲所得溶液中含有溶质的是 。
(2)根据实验数据分析,若取用金属混合物15g,加入到120g稀硫酸中,充分反应后最终得到固体质量为 。
(3)计算丙同学所得溶液中溶质的质量分数。(写出计算过程,计算结果精确到0.1%)