题目内容
7.生活中有许多俗语.下列有关说法,从化学的角度理解不正确的是( )| A. | 酒香不怕巷子深--分子不断运动 | |
| B. | 真金不怕火炼--金的金属活动性很强 | |
| C. | 千锤百炼、百炼成钢--生铁可炼成钢 | |
| D. | 火要空心--增大与空气的接触面积,能使可燃物燃烧更充分 |
分析 A.根据分子是不断运动的特性判断;
B.依据高温时金不会发生化学变化分析解答;
C.依据生铁和钢的区别对该过程进行分析即可;
D.依据物质充分燃烧时的影响因素分析解答即可.
解答 解:A.由于分子是不断运动的,酒精的分子通过运动能分散到周围的空气中,所以,酒香不怕巷子深,解释正确.
B.“真金不怕火炼”是指金在高温时也不会发生化学变化,体现了金的金属活动性较弱,解释错误.
C.“千锤百炼,百炼金钢”锤是锤打,炼是烧炼.从而反映了生铁经过以上过程会变成钢的事实,解释正确.
D.“火要空心”是指可燃物在燃烧时要充分的与空气接触,这样有利于可燃物的充分燃烧,解释正确.
故选B.
点评 此题通过联系身边的知识来考查化学中的基本规律和性质,题意较新颖,能体现化学知识的重要性.

练习册系列答案
相关题目
18.中医药是中华民族的宝贵财富,为民族的繁衍昌盛作出巨大贡献,在熬制中药的操作过程中属于化学变化的是( )
| A. | 切细药材 | B. | 浸泡药材 | C. | 熬制汤药 | D. | 滤去药渣 |
2.中国古诗词的神韵让人回味无穷.下列诗词中涉及到化学变化的是( )
| A. | 姑苏城外寒山寺,夜半钟声到客船 | B. | 千锤万凿出深山,烈火焚烧若等闲 | ||
| C. | 飞流直下三千尺,疑是银河落九天 | D. | 清明时节雨纷纷,路上行人欲断魂 |
12.下列实验操作不规范、不符合要求的是( )
| A. |  验证燃烧条件 | B. |  验证氧气体积分数 | ||
| C. |  排水收集气体 | D. |  过滤操作 |
19.自制汽水.在500mL的饮料瓶中加入2勺白糖、1.5g小苏打,注入凉开水,再加入1.5g柠檬酸(C6H8O7),立即旋紧瓶盖,摇匀.
【资料】反应原理:3NaHCO3+C6H8O7═C6H5O7Na3+3H2O+3CO2↑
请从28-A或28-B两题中任选1个作答,若两题均作答,按28-A计分.
【资料】反应原理:3NaHCO3+C6H8O7═C6H5O7Na3+3H2O+3CO2↑
请从28-A或28-B两题中任选1个作答,若两题均作答,按28-A计分.
| 28-A | 28-B |
| (1)柠檬酸中碳、氢元素的质量比为9:1. (2)制得的汽水呈酸甜口味,依据数据阐述 呈酸味的理由是通过计算,柠檬酸过量. | (1)柠檬酸中碳元素的质量分数为37.5%,其计算式为$\frac{12×6}{12×6+1×8+16×7}×100%$. (2)加入柠檬酸后,立即旋紧瓶盖的原因 是减少CO2逸出. |
8.空气中氧气含量测定的再认识.
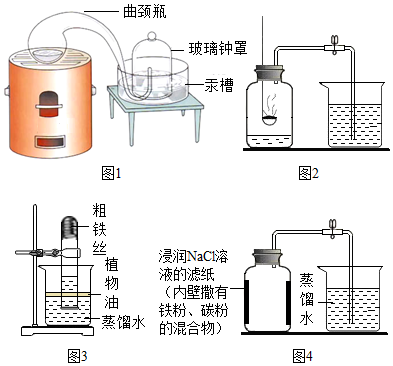
【经典赏析】教材中介绍了拉瓦锡用定量的方法研究了空气的成分(实验装置如图1).
该实验中选择使用汞的优点有BCD.
A.实验过程中没有污染
B.在汞槽中起到液封的作用
C.能将密闭装置内空气中的氧气几乎耗尽
D.生成的化合物加热分解又能得到汞和氧气
【实验回顾】实验室常用红磷燃烧的方法测定测定空气中氧气的含量(装置如图2).当冷却至室温后,集气瓶内剩余气体的成分是D.
A.五氧化二磷 B.主要成分为氦气和氧气
C.纯净的氦气 D.主要成分为氮气的混合气体
兴趣小组的同学用该方法测出的氧气含量常常远低于21%.
【提出问题】用红磷燃烧的方法为什么测定空气中氧气的含量会偏小?
【进行猜想】(1)装置漏气;(2)红磷不足装置内氧气有剩余;(3)没有冷却至室温就打开止水夹;…
【实验与交流】在老师的指导下,凤九分别用过量的红磷和白鳞进行该实验,用测定氧气浓度的传感器测得反应后装置内氧气浓度分别为8.85%和3.21%.请从燃烧条件的角度分析产生上述两个结果较大差异的主要原因是:白磷的着火点比红磷的着火点低.
【实验探究1】东华根据铁生锈的原理,探究用铁能否准确测定空气中氧气的含量.于是进行了实验(装置如图3).
通过7天测得的数据计算出空气中氧气的含量为19.13%.
【交流与反思】用于红磷燃烧的方法相比,用铁丝生锈的方法测定的主要优点是:装置内残留的氧气更少,实验结果更准确.
【实验探究2】为了加快反应速率,东华通过查阅资料,利用铁粉、炭粉、氯化钠等物质又进行了实验(装置如图4).8分钟后测得的数据如表:
请计算出空气中氧气含量为20.2%(计算结果保留一位小数).
【结论与反思】通过上述实验探究,选择铁粉、炭粉、氯化钠和蒸馏水(填物质名称)进行实验,可较为快速地完成实验并减小实验误差.
【拓展延伸】
铜也能与空气中氧气、水、二氧化碳反应而锈蚀,生成铜绿(铜绿主要成分为Cu2(OH)2CO3).写出生成铜绿的化学方程式2Cu+H2O+CO2+O2=Cu2(OH)2CO3.若将图3装置中的粗铁丝换成足量的铜丝进行实验,请判断能否比较准确地测定空气中氧气的含量,并说明理由不能;因为空气中二氧化碳含量是0.03%,铜不能将装置中的氧气耗尽(相对原子质量:C-12 O-16)

【经典赏析】教材中介绍了拉瓦锡用定量的方法研究了空气的成分(实验装置如图1).
该实验中选择使用汞的优点有BCD.
A.实验过程中没有污染
B.在汞槽中起到液封的作用
C.能将密闭装置内空气中的氧气几乎耗尽
D.生成的化合物加热分解又能得到汞和氧气
【实验回顾】实验室常用红磷燃烧的方法测定测定空气中氧气的含量(装置如图2).当冷却至室温后,集气瓶内剩余气体的成分是D.
A.五氧化二磷 B.主要成分为氦气和氧气
C.纯净的氦气 D.主要成分为氮气的混合气体
兴趣小组的同学用该方法测出的氧气含量常常远低于21%.
【提出问题】用红磷燃烧的方法为什么测定空气中氧气的含量会偏小?
【进行猜想】(1)装置漏气;(2)红磷不足装置内氧气有剩余;(3)没有冷却至室温就打开止水夹;…
【实验与交流】在老师的指导下,凤九分别用过量的红磷和白鳞进行该实验,用测定氧气浓度的传感器测得反应后装置内氧气浓度分别为8.85%和3.21%.请从燃烧条件的角度分析产生上述两个结果较大差异的主要原因是:白磷的着火点比红磷的着火点低.
【实验探究1】东华根据铁生锈的原理,探究用铁能否准确测定空气中氧气的含量.于是进行了实验(装置如图3).
通过7天测得的数据计算出空气中氧气的含量为19.13%.
【交流与反思】用于红磷燃烧的方法相比,用铁丝生锈的方法测定的主要优点是:装置内残留的氧气更少,实验结果更准确.
【实验探究2】为了加快反应速率,东华通过查阅资料,利用铁粉、炭粉、氯化钠等物质又进行了实验(装置如图4).8分钟后测得的数据如表:
| 实验前的体积 | 实验后的体积 | |
| 集气瓶内空气 | 烧杯内蒸馏水 | 烧杯内剩余蒸馏水 |
| 131mL | 90.0mL | 63.6mL |
【结论与反思】通过上述实验探究,选择铁粉、炭粉、氯化钠和蒸馏水(填物质名称)进行实验,可较为快速地完成实验并减小实验误差.
【拓展延伸】
铜也能与空气中氧气、水、二氧化碳反应而锈蚀,生成铜绿(铜绿主要成分为Cu2(OH)2CO3).写出生成铜绿的化学方程式2Cu+H2O+CO2+O2=Cu2(OH)2CO3.若将图3装置中的粗铁丝换成足量的铜丝进行实验,请判断能否比较准确地测定空气中氧气的含量,并说明理由不能;因为空气中二氧化碳含量是0.03%,铜不能将装置中的氧气耗尽(相对原子质量:C-12 O-16)
 如图是甲、乙两种固体物质的溶解度曲线.
如图是甲、乙两种固体物质的溶解度曲线. 如图是打火机的示意图.请根据有关信 息回答下列问题:
如图是打火机的示意图.请根据有关信 息回答下列问题:


