题目内容
某医院化验室欲测定一批过氧化氢溶液的浓度,取2.5g二氧化锰放入盛有85g过氧化氢溶液的锥形瓶中,反应完全结束后,测得锥形瓶内混合物的总质量为85.9g.请完成下列问题:
(1)反应生成氧气的质量为 g.
(2)这批过氧化氢溶液中溶质的质量分数是多少?
(3)如果要将这批过氧化氢溶液配置成浓度为1%的消毒液,需要加水的质量是多少?
(1)反应生成氧气的质量为
(2)这批过氧化氢溶液中溶质的质量分数是多少?
(3)如果要将这批过氧化氢溶液配置成浓度为1%的消毒液,需要加水的质量是多少?
考点:根据化学反应方程式的计算,用水稀释改变浓度的方法,有关溶质质量分数的简单计算
专题:溶质质量分数与化学方程式相结合的计算
分析:(1)根据质量守恒定律解答;
(2)根据生成氧气的质量可以计算过氧化氢溶液中过氧化氢的质量.
(3)根据稀释时溶液中溶质质量不变解答.
(2)根据生成氧气的质量可以计算过氧化氢溶液中过氧化氢的质量.
(3)根据稀释时溶液中溶质质量不变解答.
解答:解:(1)反应生成氧气的质量为:2.5g+85g-85.9g=1.6g
(2)解:设原过氧化氢溶液中过氧化氢的质量为x,
2H2O2
2H2O+O2↑,
68 32
x 1.6g
=
x=3.4g
这批过氧化氢溶液中溶质的质量分数是:
×100%=4%;
(3)设需要加水的质量为y
×100%=1%
y=255g
答:(1)反应生成氧气的质量为1.6g,
(2)这批过氧化氢溶液中溶质的质量分数是4%,
(3)需要加水的质量是255g.
(2)解:设原过氧化氢溶液中过氧化氢的质量为x,
2H2O2
| ||
68 32
x 1.6g
| 68 |
| x |
| 32 |
| 1.6g |
x=3.4g
这批过氧化氢溶液中溶质的质量分数是:
| 3.4g |
| 85g |
(3)设需要加水的质量为y
| 3.4g |
| 85g+y |
y=255g
答:(1)反应生成氧气的质量为1.6g,
(2)这批过氧化氢溶液中溶质的质量分数是4%,
(3)需要加水的质量是255g.
点评:本道题目比较简单,是一道最基本的根据化学方程式的计算题,解题关键是根据质量守恒定律求出氧气的质量.

练习册系列答案
相关题目
下列实验中,所用试剂或方法正确的是( )
| A、除去CaO中少量CaCO3:加入适量盐酸后过滤 |
| B、证明碳酸钠溶液中含氢氧化钠:加过量氯化钙溶液后加酚酞,观察是否变红 |
| C、检验集气瓶中的氧气已收满:将带火星的木条插到集气瓶底部,观察木条是否立刻剧烈燃烧 |
| D、测定某溶液的酸碱度:取少量样品,滴加紫色石蕊试液 |

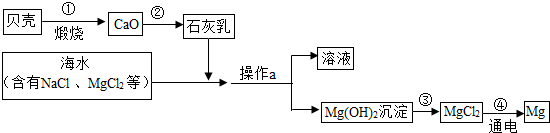
 化学兴趣小组的同学在实验室模拟工业制糖过程.
化学兴趣小组的同学在实验室模拟工业制糖过程.
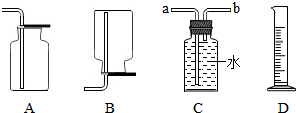 回收废旧干电池能减少对水和土壤的污染.某化学兴趣小组决定回收干电池,并以电池锌皮为原料制取氢气及相关探究实验:用锌和稀硫酸制取氢气.己知氢气密度比空气小且难溶于水,提供装置如图.
回收废旧干电池能减少对水和土壤的污染.某化学兴趣小组决定回收干电池,并以电池锌皮为原料制取氢气及相关探究实验:用锌和稀硫酸制取氢气.己知氢气密度比空气小且难溶于水,提供装置如图.