题目内容
相对原子质量和相对分子质量:
(1)查表得氧的相对原子质量为16,这说明一个氧原子的质量是16g吗?
(2)氧的相对原子质量为16的涵义是什么?
(3)相对原子质量越大的原子,其实际质量也越大吗?
(4)计算得水的相对分子质量为18,这说明一个水分子的质量是18g吗?
(5)水的相对分子质量为18的涵义是什么?
(6)相对分子质量越大的分子,其实际质量也越大吗?
(1)查表得氧的相对原子质量为16,这说明一个氧原子的质量是16g吗?
(2)氧的相对原子质量为16的涵义是什么?
(3)相对原子质量越大的原子,其实际质量也越大吗?
(4)计算得水的相对分子质量为18,这说明一个水分子的质量是18g吗?
(5)水的相对分子质量为18的涵义是什么?
(6)相对分子质量越大的分子,其实际质量也越大吗?
考点:相对原子质量的概念及其计算方法,相对分子质量的概念及其计算
专题:化学式的计算
分析:相对原子质量是一个比值,单位是1;相对原子质量的概念是以一种碳原子(即碳-12原子)质量的1/12作为标准,其它原子的质量(实际质量)跟它相比较所得的值,相对分子质量的概念是化学式中各原子的相对原子质量的总和,据此分析解答.
解答:解:(1)相对原子质量的概念是以一种碳原子(即碳-12原子)质量的1/12作为标准,其它原子的质量(实际质量)跟它相比较所得的值,则氧原子的质量是16和碳原子质量的1/12的乘积,故说法错误;
(2)由(1)分析可知:氧的相对原子质量为16表示氧原子的质量和碳原子质量的1/12的比值;
(3)通过(1)可知,碳原子质量的1/12是一个定值,原子的实际质量=相对原子质量×碳原子质量的1/12,所以相对原子质量越大,其实际质量也越大;
(4)相对分子质量的概念是化学式中各原子的相对原子质量的总和,所以水的相对分子质量为18表示其分子中各原子的相对原子质量的总和是18,而不是水分子的实际质量;
(5)水的相对分子质量为18表示其分子中各原子的相对原子质量的总和是18;
(6)相对分子质量越大,则其实际质量越大;
故答案为:(1)氧原子的质量是16和碳原子质量的1/12的乘积;
(2)氧的相对原子质量为16表示氧原子的质量和碳原子质量的1/12的比值;
(3)相对原子质量越大,其原子的实际质量也越大;
(4)水的相对分子质量为18表示其分子中各原子的相对原子质量的总和是18,而不是水分子的实际质量;
(5)水的相对分子质量为18表示其分子中各原子的相对原子质量的总和是18;
(6)相对分子质量越大,则其实际质量越大.
(2)由(1)分析可知:氧的相对原子质量为16表示氧原子的质量和碳原子质量的1/12的比值;
(3)通过(1)可知,碳原子质量的1/12是一个定值,原子的实际质量=相对原子质量×碳原子质量的1/12,所以相对原子质量越大,其实际质量也越大;
(4)相对分子质量的概念是化学式中各原子的相对原子质量的总和,所以水的相对分子质量为18表示其分子中各原子的相对原子质量的总和是18,而不是水分子的实际质量;
(5)水的相对分子质量为18表示其分子中各原子的相对原子质量的总和是18;
(6)相对分子质量越大,则其实际质量越大;
故答案为:(1)氧原子的质量是16和碳原子质量的1/12的乘积;
(2)氧的相对原子质量为16表示氧原子的质量和碳原子质量的1/12的比值;
(3)相对原子质量越大,其原子的实际质量也越大;
(4)水的相对分子质量为18表示其分子中各原子的相对原子质量的总和是18,而不是水分子的实际质量;
(5)水的相对分子质量为18表示其分子中各原子的相对原子质量的总和是18;
(6)相对分子质量越大,则其实际质量越大.
点评:了解相对原子质量和相对分子质量的计算方法是解答此题的基础.

练习册系列答案
 快乐5加2金卷系列答案
快乐5加2金卷系列答案
相关题目
在天平两端各放一个盛有等质量等质量分数的稀硫酸的烧杯,调天平至平衡,若分别投入镁粉和铁粉,且全部溶解,天平仍保持平衡,则投入镁粉和铁粉的质量比为( )
| A、3:7 | B、7:3 |
| C、77:81 | D、81:77 |
下列关于酸、碱、盐的元素组成,叙述正确的是( )
| A、正盐可能含氢元素 |
| B、酸和碱的组成中一定含氢元素和氧元素 |
| C、酸、正盐、酸式盐一定含氢元素 |
| D、酸、碱、盐都可能不含金属元素 |
下列关于原子的说法,错误的是( )
| A、原子是化学变化中最小的粒子 |
| B、原子都是由质子、中子、电子构成 |
| C、原子核带正电荷,但原子不显电性 |
| D、在原子中,核电荷数=质子数=电子数 |
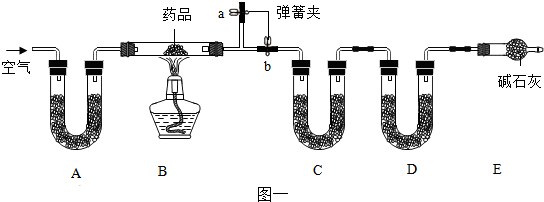
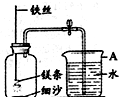 某校研究性学习小组用如图装置进行镁条在空气中燃烧的实验,燃烧、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶体积的70%.
某校研究性学习小组用如图装置进行镁条在空气中燃烧的实验,燃烧、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶体积的70%. A、B、C三种固体物质的溶解度如右图所示,根据图答题:
A、B、C三种固体物质的溶解度如右图所示,根据图答题: