题目内容
下列关于原子的说法,错误的是( )
| A、原子是化学变化中最小的粒子 |
| B、原子都是由质子、中子、电子构成 |
| C、原子核带正电荷,但原子不显电性 |
| D、在原子中,核电荷数=质子数=电子数 |
考点:原子的定义与构成
专题:物质的微观构成与物质的宏观组成
分析:根据原子在化学变化中不可再分,氢原子核内没有中子,原子核是由质子和中子构成,质子带正电荷,中子不带电,故原子核带正电荷,但由于原子核与核外电子所带电荷数量相等,电性相反,故整个原子不显电性进行解答.
解答:解:A、原子在化学变化中不可再分,是化学变化中的最小微粒,故A正确;
B、氢原子核内没有中子,故B错误;
C、原子核是由质子和中子构成,质子带正电荷,中子不带电,故原子核带正电荷,但由于原子核与核外电子所带电荷数量相等,电性相反,故整个原子不显电性,故C正确;
D、在原子中,原子核是由质子和中子构成,质子带正电荷,中子不带电,故原子核带正电荷,但由于原子核与核外电子所带电荷数量相等,电性相反,故核电荷数=质子数=电子数正确;
故选:B.
B、氢原子核内没有中子,故B错误;
C、原子核是由质子和中子构成,质子带正电荷,中子不带电,故原子核带正电荷,但由于原子核与核外电子所带电荷数量相等,电性相反,故整个原子不显电性,故C正确;
D、在原子中,原子核是由质子和中子构成,质子带正电荷,中子不带电,故原子核带正电荷,但由于原子核与核外电子所带电荷数量相等,电性相反,故核电荷数=质子数=电子数正确;
故选:B.
点评:本题考查了原子的有关知识,完成此题,可以依据已有的知识进行.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
CO2通人石蕊试液中,颜色会变红是因为( )
| A、CO2可与水反应生成H2CO3 |
| B、CO2微溶于水 |
| C、CO2与石蕊反应 |
| D、CO2吸附水中的色素 |
“NaCl+CO2+NH3+H2O═NaHCO3↓+NH4Cl”是著名的”侯氏制碱法“的重要反应.下面是4位同学对该反应涉及的有关知识发表的部分见解.其中不正确的是( )
| A、甲同学说:该条件下NaHCO3的溶解度较大 |
| B、乙同学说:NaHCO3不是纯碱 |
| C、丙同学说:析出NaHCO3固体后的溶液为碳酸氢钠的饱和溶液 |
| D、丁同学说:从该反应可以获得氮肥 |
今有四种粒子的结构示意图,下列说法不正确的是( )


| A、它们表示四种元素 |
| B、④表示的元素在化合物通常显+3价 |
| C、①表示的粒子在化学反应中易得到电子 |
| D、②③都表示阴离子 |
下列物质之间的转化,不能通过一步反应实现的是( )
| A、Fe→FeCl3 |
| B、CuO→CuSO4 |
| C、Na2CO3→NaCl |
| D、NaOH→H2O |


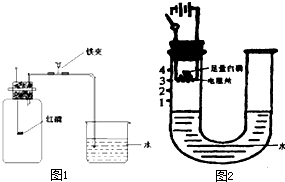 在“空气中氧气含量的测定”实验探究中,小涵设计了如下实验方案:在燃烧匙内盛过量红磷,点燃后立即插入集气瓶内,塞紧橡皮塞,待红磷火焰熄灭,集气瓶冷却至室温,打开铁夹,水注入集气瓶.已知红磷和白磷的化学性质相似,二氧化硫能与氢氧化钠溶液反应生成亚硫酸钠固体和水,亚硫酸钠固体能溶于水.(实验装置如图1所示)回答下列问题:
在“空气中氧气含量的测定”实验探究中,小涵设计了如下实验方案:在燃烧匙内盛过量红磷,点燃后立即插入集气瓶内,塞紧橡皮塞,待红磷火焰熄灭,集气瓶冷却至室温,打开铁夹,水注入集气瓶.已知红磷和白磷的化学性质相似,二氧化硫能与氢氧化钠溶液反应生成亚硫酸钠固体和水,亚硫酸钠固体能溶于水.(实验装置如图1所示)回答下列问题: