题目内容
10.如图是两个实验小组分别进行“加热硫酸铜和氢氧化钠溶液反应后生成物”的实验过程示意图: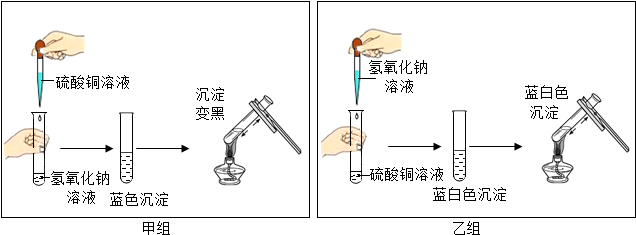
【甲组】氢氧化钠与硫酸铜反应的化学方程式为2NaOH+CuSO4=Na2SO4+Cu(OH)2↓,加热后产生黑色的氧化铜.
【乙组】为寻找实验中没有产生氧化铜的原因,他们进行了以下实验探究:
【查阅资料】在酸性条件下,氢氧化钠与硫酸铜在溶液中可发生如下反应:
6NaOH+4CuSO4═3Na2SO4+Cu4(OH)6SO4↓,生成的碱式硫酸铜是不溶于水的蓝白色固体,加热不易发生分解.
【提出猜想】根据资料分析,同学们针对试管中溶液呈酸性的原因作出以下猜想:
猜想Ⅰ:硫酸铜溶液呈酸性; 猜想Ⅱ:生成的硫酸钠使溶液呈酸性.
【实验与结论】
实验①:用pH试纸测定硫酸铜溶液的酸碱度,得出其pH<(填“>”、“<”或“﹦”),硫酸铜溶液呈酸性,猜想Ⅰ成立.
实验②:向盛有硫酸钠溶液的试管中逐滴加石蕊溶液,观察到溶液显紫色,硫酸钠溶液呈中(填“酸”、“中”或“碱”)性,猜想Ⅱ不成立.
【交流和反思】(1)乙组同学认真分析甲组实验后,一致认为不需要通过实验就能判断猜想Ⅱ不成立,理由是甲组实验生成了Na2SO4,若它显酸性,在此条件下氢氧化钠与硫酸铜反应会生成蓝白色沉淀;
(2)在化学反应中,相同的反应物因质量比不同可能会导致生成物不同,请另举一列碳与氧气(写出反应物即可).
分析 【甲组】根据氢氧化钠和硫酸铜反应生成氢氧化铜沉淀和硫酸钠进行分析;
【实验与结论】根据提出的猜想和题中进行的实验进行分析;
【交流和反思】(1)根据在酸性条件下,氢氧化钠与硫酸铜在溶液中可发生反应会生成不溶于水的蓝白色固体碱式硫酸铜进行分析;
(2)根据碳和充足的氧气反应生成二氧化碳,和不足的氧气反应生成一氧化碳进行分析.
解答 解:【甲组】氢氧化钠和硫酸铜反应生成氢氧化铜沉淀和硫酸钠,化学方程式为:2NaOH+CuSO4=Na2SO4+Cu(OH)2↓;
【实验与结论】实验①:用pH试纸测定硫酸铜溶液的酸碱度,得出其pH<7,硫酸铜溶液呈酸性,猜想Ⅰ成立;
实验②:向盛有硫酸钠溶液的试管中逐滴加石蕊溶液,观察到溶液显紫色,硫酸钠溶液呈中性,猜想Ⅱ不成立;
【交流和反思】(1)在酸性条件下,氢氧化钠与硫酸铜在溶液中可发生反应会生成不溶于水的蓝白色固体碱式硫酸铜,所以乙组同学认真分析甲组实验后,一致认为不需要通过实验就能判断猜想Ⅱ不成立;
(2)碳和充足的氧气反应生成二氧化碳,和不足的氧气反应生成一氧化碳.
故答案为:【甲组】2NaOH+CuSO4=Na2SO4+Cu(OH)2↓;
【实验与结论】实验①<;
实验②:中;
【交流和反思】(1)甲组实验生成了Na2SO4,若它显酸性,在此条件下;
(2)碳与氧气.
点评 在解此类题时,首先分析题中考查的问题,然后结合学过的知识和题中的提示进行解答.

练习册系列答案
相关题目
1.下列实验操作正确且能达到实验目的是( )
| A. |  连接仪器 | B. |  过滤 | C. |  稀释浓硫酸 | D. |  检查气密性 |
5. 如图是小凡用手势OK表示初中常见化学反应中生成水的不同方法,要求手指上的物质分别通过某种反应的基本类型直接生成水(如图中的H2O2、O2)则物质X一定不是下列物质中的( )
如图是小凡用手势OK表示初中常见化学反应中生成水的不同方法,要求手指上的物质分别通过某种反应的基本类型直接生成水(如图中的H2O2、O2)则物质X一定不是下列物质中的( )
 如图是小凡用手势OK表示初中常见化学反应中生成水的不同方法,要求手指上的物质分别通过某种反应的基本类型直接生成水(如图中的H2O2、O2)则物质X一定不是下列物质中的( )
如图是小凡用手势OK表示初中常见化学反应中生成水的不同方法,要求手指上的物质分别通过某种反应的基本类型直接生成水(如图中的H2O2、O2)则物质X一定不是下列物质中的( )| A. | H2 | B. | H2CO3 | C. | CH4 | D. | KOH |
15.下列化学用语与意义对应不相符的是( )
| A. | O2:一个氧分子 | |
| B. | 4Ne:4个氖原子 | |
| C. | SiO2:二氧化硅 | |
| D. | 2Mg2+:两个镁离子带两个单位的正电荷 |
2.诺贝尔奖获得者屠呦呦发现的青蒿素,化学式C15H22O5,下列关于青蒿素的说法错误的是( )
| A. | 青蒿素是一种氧化物 | B. | 青蒿素由碳、氢、氧三种元素组成 | ||
| C. | 每个青蒿素分子中含有42个原子 | D. | 青蒿素中碳元素的质量分数最大 |
20.下列实验操作正确的是( )
| A. |  取下刚加热后的蒸发皿 | B. |  稀释浓硫酸 | ||
| C. |  熄灭酒精灯 | D. |  向上排空气法收集二氧化碳 |
 根据原子结构示意图和微观示意图填空
根据原子结构示意图和微观示意图填空
 联系学过的化学知识,回答下列问题:
联系学过的化学知识,回答下列问题: