题目内容
13.硝酸铵(NH4NO3)是一种常见的氮肥,下列关于硝酸铵说法正确的是( )| A. | 共含4种元素 | B. | 氮元素化合价是+1价 | ||
| C. | 氮、氢、氧原子个数比是2:4:3 | D. | 氮肥硝酸铵能与碱性物质滥用 |
分析 A、根据硝酸铵的化学式的意义进行分析;
B、根据化合物中各元素化合价代数和为零进行分析;
C、根据化合物化学式的意义进行分析;
D、根据铵态氮肥不能与碱性物质混用进行分析.
解答 解:A、硝酸铵是由氮、氢、氧三种元素组成的,故说法错误;
B、硝酸铵中,铵根中氮元素的化合价为-3价,硝酸根中氮元素的化合价是+5,故说法错误;
C、硝酸铵中氮、氢、氧原子个数比是2:4:3,故说法正确.
D、硝酸铵属于铵态氮肥,加碱有刺激性气味的氨气产生,从而降低肥效,因此硝酸铵不能与碱性物质混用,故说法错误.
故选:C.
点评 本题难度不大,考查学生对化学式含义的理解、铵态氮肥的性质等进行分析解题的能力.

练习册系列答案
相关题目
3. 在元素周期表中锡元素的某些信息如图所示,下列有关锡的说法正确的是( )
在元素周期表中锡元素的某些信息如图所示,下列有关锡的说法正确的是( )
 在元素周期表中锡元素的某些信息如图所示,下列有关锡的说法正确的是( )
在元素周期表中锡元素的某些信息如图所示,下列有关锡的说法正确的是( )| A. | 原子序数为50 | B. | 属于非金属元素 | ||
| C. | 相对原子质量是118.7g | D. | 原子核内中子数为50 |
4. 王小彤同学在2012年春节期间帮忙厨师剥山药皮后发现,山药削皮后,与空气中的氧化合变成褐色,他感觉很惊奇,查阅资料后才知道这种变化称为食物的酶促褐变.不仅苹果、梨子有这种情况,有些蔬菜(如土豆、茄子等)也有这种情况.如去皮的芋艿在自然条件下,表面也很快因氧化而变黄色,但并不影响营养价值.有些不法商贩会用亚硫酸钠溶液浸泡.便其外观变得嫩白,造成食品安全问题.下面做法也会带来食品安全问题的是( )
王小彤同学在2012年春节期间帮忙厨师剥山药皮后发现,山药削皮后,与空气中的氧化合变成褐色,他感觉很惊奇,查阅资料后才知道这种变化称为食物的酶促褐变.不仅苹果、梨子有这种情况,有些蔬菜(如土豆、茄子等)也有这种情况.如去皮的芋艿在自然条件下,表面也很快因氧化而变黄色,但并不影响营养价值.有些不法商贩会用亚硫酸钠溶液浸泡.便其外观变得嫩白,造成食品安全问题.下面做法也会带来食品安全问题的是( )
 王小彤同学在2012年春节期间帮忙厨师剥山药皮后发现,山药削皮后,与空气中的氧化合变成褐色,他感觉很惊奇,查阅资料后才知道这种变化称为食物的酶促褐变.不仅苹果、梨子有这种情况,有些蔬菜(如土豆、茄子等)也有这种情况.如去皮的芋艿在自然条件下,表面也很快因氧化而变黄色,但并不影响营养价值.有些不法商贩会用亚硫酸钠溶液浸泡.便其外观变得嫩白,造成食品安全问题.下面做法也会带来食品安全问题的是( )
王小彤同学在2012年春节期间帮忙厨师剥山药皮后发现,山药削皮后,与空气中的氧化合变成褐色,他感觉很惊奇,查阅资料后才知道这种变化称为食物的酶促褐变.不仅苹果、梨子有这种情况,有些蔬菜(如土豆、茄子等)也有这种情况.如去皮的芋艿在自然条件下,表面也很快因氧化而变黄色,但并不影响营养价值.有些不法商贩会用亚硫酸钠溶液浸泡.便其外观变得嫩白,造成食品安全问题.下面做法也会带来食品安全问题的是( )| A. | 海产品用甲醛溶液保鲜 | B. | 食盐中加碘防止甲状腺肿大 | ||
| C. | 食品袋内充入氮气使其不易变质 | D. | 用纯碱作为发酵剂做馒头 |
1.下列属于物质化学性质的是( )
| A. | 溶解性 | B. | 可燃性 | C. | 挥发性 | D. | 导电性 |
8.下列归纳和总结完全正确的一组是( )
| A对除杂的认识 | B对知识的应用 |
| ①用点燃的方法除去CO2中的CO ②用溶解、过滤、蒸发除去氯化钠中的泥沙 ③用冷却热的饱和溶液除硝酸钾中少量氯化钠 | ①厨房洗涤剂可以乳化餐具上的油污 ②液化气泄漏时关闭阀门并开窗通风 ③施肥时氯化铵不能与草木灰混合施用 |
| C对现象的描述 | D对概念的理解 |
| ①铁丝在空气中剧烈燃烧,火星四射 ②打开浓盐酸瓶盖有白烟 ③电解水生成氢气和氧气的体积比约为2:1 | ①生成盐和水的反应一定是中和反应 ②燃烧生成二氧化碳的物质一定含碳元素 ③使紫色石蕊溶液变蓝的一定是碱性溶液 |
| A. | A | B. | B | C. | C | D. | D |
18.下列四个图象分别表示对应的四种操作过程,其中表示正确的图象是( )
| A. | 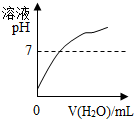 向pH=2的酸溶液中不断加水 | |
| B. | 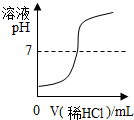 向NaOH溶液中逐滴加入稀盐酸 | |
| C. | 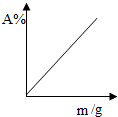 向一定量的水中持续加入食盐(m表示食盐的质量,A%表示溶质分数) | |
| D. | 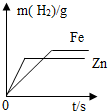 等质量的锌、铁与足量的稀硫酸反应,产生氢气的质量随反应时间t的变化 |
5.工业上用甲和乙通过化合反应制备丙,下列是三种分子的模型图,根据下列微观示意图得出的结论错误的是( )


| A. | 甲的化学式为C2H4 | |
| B. | 保持乙化学性质的最小微粒是水分子 | |
| C. | 乙和丙都属于氧化物 | |
| D. | 在化学变化中分子分成原子,原子又重新组合成新物质的分子 |
2. 为测定12g含杂质的氧化铁样品中氧化铁的质量分数,利用稀硫酸和锌粒制取氢气,设计了如图所示的装置,进行有关的实验探究(提示:3H2+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3H2O杂质不参加反应,假定每步均完全反应或吸收).请回答有关问题:
为测定12g含杂质的氧化铁样品中氧化铁的质量分数,利用稀硫酸和锌粒制取氢气,设计了如图所示的装置,进行有关的实验探究(提示:3H2+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3H2O杂质不参加反应,假定每步均完全反应或吸收).请回答有关问题:
得到洗礼数据
(请计算样品中氧化铁的质量分数.(写出计算步骤,计算结果精确到0.1%)
 为测定12g含杂质的氧化铁样品中氧化铁的质量分数,利用稀硫酸和锌粒制取氢气,设计了如图所示的装置,进行有关的实验探究(提示:3H2+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3H2O杂质不参加反应,假定每步均完全反应或吸收).请回答有关问题:
为测定12g含杂质的氧化铁样品中氧化铁的质量分数,利用稀硫酸和锌粒制取氢气,设计了如图所示的装置,进行有关的实验探究(提示:3H2+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3H2O杂质不参加反应,假定每步均完全反应或吸收).请回答有关问题:得到洗礼数据
| 装置 | B | C |
| 反应前的质量 | 86.3g | 284.2g |
| 反应后的质量 | 83.9g | 286.9g |
3.小惠周末帮妈妈做家务时,发现厨房里有一包无标识的白色粉末,经询问得知可能是食盐、纯碱或小苏打.于是,小惠取一些带回学校实验室与同学一起对白色粉末的成分进行了探究.
【提出猜想】
猜想1:可能是食盐;
猜想2:可能是纯碱;
猜想3:可能是小苏打.
【查阅资料】小苏打的性质:①水溶液呈碱性;②受热易分解;③能跟氢氧化钠溶液发生反应:NaHCO3+NaOH═Na2CO3+H2O.
【实验探究】小惠取适量白色粉末,配制成溶液,按如表进行实验:
【讨论交流】同学们认为通过上述实验无法确定白色粉末的成分,原因是碳酸钠和碳酸氢钠都能与盐酸反应生成使澄清的石灰水变浑浊的气体;实验步骤②中可能发生反应的化学方程式是Na2CO3+2HCl═2NaCl+H2O+CO2↑(写一个);实验步骤③中白色沉淀的成分是CaCO3(填写化学式).
【继续探究】小惠用试管另取少量白色粉末,管口套上带导管的单孔橡皮塞,将导管末端插入澄清石灰水中,给试管加热,观察到石灰水未变浑浊,得出该白色粉末是碳酸氢钠.
【实验反思】有同学提出:该白色粉末如果放置了较长时间且未密封保存,刚买时也可能是猜想中的另一种物质,理由是厨房温度高,小苏打受热易分解.
【提出猜想】
猜想1:可能是食盐;
猜想2:可能是纯碱;
猜想3:可能是小苏打.
【查阅资料】小苏打的性质:①水溶液呈碱性;②受热易分解;③能跟氢氧化钠溶液发生反应:NaHCO3+NaOH═Na2CO3+H2O.
【实验探究】小惠取适量白色粉末,配制成溶液,按如表进行实验:
| 步骤 | 实验内容 | 实验现象 | 实验结论 |
| ① | 取少量溶液,滴加无色酚酞溶液 | 溶液变红色 | 白色粉末肯定不是NaCl |
| ② | 取少量溶液,滴加稀盐酸 | 有气泡产生 | / |
| ③ | 取少量溶液,滴加澄清石灰水 | 产生白色沉淀 | / |
【继续探究】小惠用试管另取少量白色粉末,管口套上带导管的单孔橡皮塞,将导管末端插入澄清石灰水中,给试管加热,观察到石灰水未变浑浊,得出该白色粉末是碳酸氢钠.
【实验反思】有同学提出:该白色粉末如果放置了较长时间且未密封保存,刚买时也可能是猜想中的另一种物质,理由是厨房温度高,小苏打受热易分解.