��Ŀ����
9���������ͼ�ش��������⣺
��1��ָ�����б�����������ƣ�Y����̨��Z����©����
��2��ʵ����ijͬѧ�ø������Ϊԭ����ȡ����ʱ��Ӧѡ��A����װ�ñ�� ��������װ�ã��÷�Ӧ�ķ��ű���ʽΪ��2KMnO4$\frac{\underline{\;\;��\;\;}}{\;}$K2MnO4+MnO2+O2�������ռ�һƿ������������������ȼ�յ�ʵ��ʹ�ã����ѡ��������ռ�װ���е�D����װ����ţ���������ˮ���ռ�������Ϻ����������������������ɵĺ����ˮ�ᵹ����
��ը���Թܣ������������ˮ���ڵ�ˮ�Ժ�ɫ�������������һ��ԭ���ǣ��Թܿ�û�з����ţ�
��3��ijͬѧ�ù���������Һ�ڶ������̵�����������������װ��C��E���ӣ�ʵ�鿪ʼһ��ʱ���������ľ�����뼯��ƿ�ڲ����ײ�������ȼ��ԭ���dz���©�����¿���Һ�����ϣ�û���ռ���������
��4�����ͬѧ����װ��F���ռ�����������Ӧ�ô�a����ܱ��a��b����ͬ��ͨ�룬����װ��BFG������ⶨ����������Һ���������������Ӧ���ڼ���ƿ��װ��ˮ��Ȼ����a��c�������ӣ�
���� ����̨�dz��õļг�����������©�������Һ��ҩƷ����ȡװ�ð������ȺͲ���������֣������˫��ˮ�Ͷ��������������Ͳ���Ҫ���ȣ�����ø�����ػ����������������Ҫ���ȣ��������ܶȱȿ������ܶȴ�������ˮ��������������ſ���������ˮ���ռ���ʵ�鿪ʼһ��ʱ���������ľ�����뼯��ƿ�ڲ����ײ�������ȼ��ԭ���ǣ�����©�����¿���Һ�����ϣ�û���ռ������������ͬѧ����װ��F���ռ�����������Ӧ�ôӳ��ܽ��룬��Ϊ�������ܶȱȿ������ܶȴ�����װ��BFG������ⶨ����������Һ���������������Ӧ���ڼ���ƿ��װ��ˮ��Ȼ����a��c�������Ӽ��ɣ�
��� �⣺��1������̨�dz��õļг�����������©�������Һ��ҩƷ���ʴ�Ϊ������̨������©����
��2������ø����������������Ҫ���ȣ�����������ȷֽ���������غͶ������̺�������Ҫע����ƽ���������ܶȱȿ������ܶȴ�������ˮ��������������ſ���������ˮ���ռ���������������ȼ�յ�ʵ��ʹ�ã����ѡ��������ռ�װ���е���ˮ�����������Թܵײ�������ˮ��ʵ�����Ӧ���Ƴ����ܣ���Ϩ��ƾ��ƣ���ԭ���ǣ���ֹˮ������ʹ�Թ�ը�ѣ������������ˮ���ڵ�ˮ�Ժ�ɫ��ԭ���ǣ��Թܿ�û�з����ţ��ʴ�Ϊ��A��2KMnO4$\frac{\underline{\;\;��\;\;}}{\;}$K2MnO4+MnO2+O2����D��ˮ�ᵹ������ը���Թܣ��Թܿ�û�з����ţ�
��3��ʵ�鿪ʼһ��ʱ���������ľ�����뼯��ƿ�ڲ����ײ�������ȼ��ԭ���ǣ�����©�����¿���Һ�����ϣ�û���ռ����������ʴ�Ϊ������©�����¿���Һ�����ϣ�û���ռ���������
��4�����ͬѧ����װ��F���ռ�����������Ӧ�ôӳ��ܽ��룬��Ϊ�������ܶȱȿ������ܶȴ�����װ��BFG������ⶨ����������Һ���������������Ӧ���ڼ���ƿ��װ��ˮ��Ȼ����a��c�������Ӽ��ɣ��ʴ�Ϊ��a��a��
���� ��������Ҫ���������������ơ��������ȡװ�ú��ռ�װ�õ�ѡ��ͬʱҲ�����˻�ѧ����ʽ����д��ע������ȣ��ۺ��ԱȽ�ǿ���������ȡװ�õ�ѡ���뷴Ӧ���״̬�ͷ�Ӧ�������йأ�������ռ�װ�õ�ѡ����������ܶȺ��ܽ����йأ����������п�����Ҫ����֮һ����Ҫ������ʵ�����У�

 ��У����ϵ�д�
��У����ϵ�д�| A�� | CaCl2 KOH Na2CO3 | B�� | K2CO3 BaCl2 HCl | ||
| C�� | K2SO4 H2SO4 NaOH | D�� | CuSO4 HNO3 NaCl |
| �¶�/�� | 0 | 20 | 40 | 60 |
| �ܽ��/g | 27.6 | 34.0 | 40.0 | 45.5 |
��2������268g 20��ʱ���Ȼ��ر�����Һ����Ҫˮ���Ȼ��ظ����ٿˣ�
��3����268��20��ʱ���Ȼ��ر�����Һ������60��ʱ������Ҫ������ٿ��Ȼ��ز��ܴﵽ����״̬��
| A�� |  ����Һ�� | B�� |  Ϩ��ƾ��� | C�� |  �㵹Һ�� | D�� |  CO2���� |
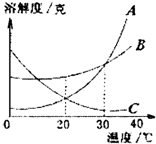 ��ͼ��ʾΪA��B��C����ͬ�����ʵ��ܽ�����ߣ�
��ͼ��ʾΪA��B��C����ͬ�����ʵ��ܽ�����ߣ� ͼΪһ����̼��ԭ����ͭ��װ��ͼ��
ͼΪһ����̼��ԭ����ͭ��װ��ͼ�� ��ͼ��ʾ�������������ȷ������ӷ�����ƿ��һ��ʱ��۲����ش��������⣺
��ͼ��ʾ�������������ȷ������ӷ�����ƿ��һ��ʱ��۲����ش��������⣺