题目内容
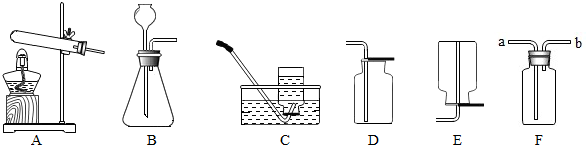
14.实验室利用如图所示装置进行相关实验,请回答下列问题:
(1)①②中属于加热仪器的是酒精灯(填名称).从A-F装置中有一个装置是错误的,改进方法是A装置中试管口应该略向下倾斜.
(2)若用高锰酸钾制取氧气,应选用的发生装置是A(填字母);实验结束后,某同学发现水槽中的水变成了浅紫红色,从实验操作角度分析其原因是试管口未放棉花;若用B和C装置制取氧气,B中发生反应的化学方程式:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(3)若要制取二氧化碳,选用的块状固体药品为大理石或石灰石;若用F装置检验二氧化碳,应在其中装入适量的澄清石灰水,出现浑浊(或白色沉淀)现象时,证明有二氧化碳产生.
(4)若要制取氢气,可以使用D或E装置收集的原因是氢气密度比空气小(或氢气难溶于水).
分析 (1)要熟悉各种仪器的名称、用途和使用方法;
为了防止水蒸气冷凝、回流炸裂试管,试管口应该略向下倾斜;
(2)高锰酸钾受热时能够分解生成锰酸钾、二氧化锰和氧气;
为了防止高锰酸钾进入导管,通常在试管口塞一团棉花;
通常情况下,过氧化氢在二氧化锰的催化作用下,分解生成水和氧气;
(3)实验室通常用大理石或石灰石和稀盐酸反应制取二氧化碳;二氧化碳能使澄清石灰水变浑浊;
(4)氢气难溶于水,密度比空气小.
解答 解:(1)属于加热仪器的是酒精灯;
A装置有错误,错误是试管口向上倾斜,应该改为试管口略向下倾斜.
(2)用高锰酸钾制取氧气需要加热,属于固体加热型,应选用的发生装置是A装置;
从实验操作角度分析其原因是:试管口处未放一小团蓬松的棉花团,导致高锰酸钾粉末进入水槽;
若用B和C装置制取氧气,是用过氧化氢制取氧气,不需加热,B中发生反应的化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(3)若要制取二氧化碳,选用的块状固体药品为大理石或石灰石;
若用F装置检验二氧化碳,应在其中装入适量的澄清石灰水,出现浑浊或白色沉淀时,证明有二氧化碳产生;
(4)若要制取氢气,可以使用D或E装置收集的原因是氢气的密度比空气小,或氢气难溶于水,且不与水反应;
故答案为:(1)酒精灯;A装置中试管口应该略向下倾斜;
(2)A;试管口未放棉花;2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(3)大理石(或石灰石);澄清石灰水;浑浊(或白色沉淀);
(4)氢气密度比空气小(或氢气难溶于水).
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要掌握相关知识,才能学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案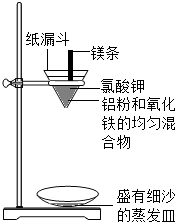 铝粉和氧化铁粉末反应(铝热反应).实验装置如图:
铝粉和氧化铁粉末反应(铝热反应).实验装置如图:图中纸漏斗由两张滤纸折叠成漏斗状套在一起,使四周都有四层,点燃镁条后观察到的现象:镁条剧烈燃烧,发出耀眼的白光,放出大量的热,纸漏斗的下部被烧穿,有熔融物落入细沙中.
实验后老师作了如下提示:实验中镁条和氯酸钾的作用是提供反应所需的高温条件,铝粉和氧化铁粉末在高温条件下的反应叫铝热反应,属于置换反应,该反应常用于焊接钢轨.请写出该反应的化学方程式2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3.该反应中单质铝与一氧化碳有相似的还原(填“氧化”或“还原”)性.在这一实验过程中没有涉及的基本反应类型是复分解反应.
实验后同学们对金属与金属氧化物间的反应产生兴趣,激发了探究热情.
【提出问题】任何金属与金属氧化物在高温条件下都能反应吗?
同学们在请教老师后设计了如下实验方案并进行了探究.
【实验方案】
| 实验组别 | 实验操作 | 实验现象 | 结论 |
| 实验1 | 取Zn、CuO粉末的均匀混合物于密闭容器中,高温加热. 向冷却后的固体中加入足量的稀盐酸. | 黑色粉末变成红色固体部分溶解,有气泡产生,水溶液呈无色. | Zn和CuO能发生置换反应. |
| 实验2 | 取Mg、CuO粉末的均匀混合物于密闭容器中,高温加热. 向冷却后的固体中加入足量的稀盐酸. | 发生爆炸,黑色粉末变成红色. 固体部分溶解,有气泡产生,水溶液呈无色. | Mg和CuO能反应 |
| 实验3 | 取Cu、Fe2O3粉末的均匀混合物于密闭容器中,高温加热. | 粉末无变化 | Cu、Fe2O3不能反应. |

| A. | 生成物一定是混合物 | |
| B. | 该反应既不是化合反应也不是分解反应 | |
| C. | 分子在化学变化中不可分 | |
| D. | 化学反应前后原子的种类不变 |
| A. | 汽油 | B. | 稀盐酸 | C. | 酒精 | D. | 水 |
| A. | 丁酸乙酯是由20个原子构成的 | |
| B. | 丁酸乙酯中碳元素的质量分数为27.6% | |
| C. | 一个丁酸乙酯分子中,碳、氢、氧原子的个数比为3:6:2 | |
| D. | 丁酸乙酯中碳、氢、氧三种元素的质量比为18:3:8 |
| A. |  向氯化铁和稀盐酸的混合溶液中不断加氢氧化钠溶液 | |
| B. |  等质量的碳酸钠粉末和块状碳酸钙分别与等体积等浓度足量的盐酸反应 | |
| C. |  向一定量的碳酸钠溶液中逐渐加水稀释 | |
| D. |  向一定量的实验室废液(实验室制取二氧化碳后产生的)中逐滴滴加碳酸钠溶液 |