题目内容
14.生活中处处有化学,现有以下常见的物质:A.明矾 B.活性炭 C.天然气 D.石墨 E.干冰
请按要求填空(填上述相应物质的字母,不重复使用):
(1)目前我市正在推广使用的清洁燃料是C;(2)常用于冰箱除臭的是B;
(3)用于冷藏保存食品的是E; (4)用于野外净水的是A;
(5)可用作电池电极的是D.
分析 可以从物质的性质和用途方面进行分析、考虑,从而得出正确的结论.
解答 解:(1)天然气是一种清洁燃料.故填:C
(2)活性炭具有吸附性.故填:B
(3)冰升华吸热可用于冷藏保存食品.故填:E
(4)明矾常常用来净化水,用于野外净水故填:A;
(5)石墨易导电,可用作电池电极.故填:D
答案:(1)C;(2)B;(3)E;(4)A;(5)D.
点评 本题主要考查物质的性质和用途,物质具有多种性质,解答时应该理解物质的用途是由物质的哪种性质决定的.

练习册系列答案
相关题目
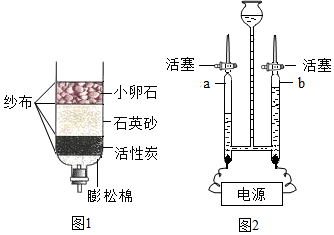
5.甲乙小组按如图1所示实验探究蜡烛的燃烧产物,获得了不同的实验现象.
甲组:烧杯内壁有无色液滴
乙组:烧杯内壁有无色液滴,烧杯底部附着有黑色固体
【提出问题】同学们查阅教材实验,得知无色液滴是水,
但黑色固体是什么呢?
【提出猜想】黑色固体是碳
【实验验证】利用如图2所示装置,甲,乙小组的同学分别设计了以下方案进行验证.
【分析与结论】
(1)实验结束时,停止通入气体,后续实验操作顺序应是BA(填字母序号).
A.熄灭酒精灯,停止加热 B.将试管b移走
(2)b中的实验现象说明黑色固体燃烧生成了二氧化碳,由此可推断猜想正确,理由是化学反应前后元素种类不变,二氧化碳的碳元素一定来自黑色固体.
【实验反思】
(1)进一步实验发现,罩在火焰上方的烧杯位置越低,产生黑色固体越多.查阅资料可知:蜡烛+氧气(足量)→二氧化碳+水;蜡烛+氧气(少量)→一氧化碳+水;…(反应条件均为“点燃”)由此推测乙组实验产生黑色固体的原因是烧杯位置降低使氧气的量减少,氧气的量少到一定程度时蜡烛和氧气反应产生黑色固体碳.
(2)甲、乙小组最终证明了蜡烛中一定含有C(填字母序号).
A.碳、氢和氧三种元素B.碳和氧两种元素C.碳和氢两种元素
(3)石蜡的主要成分为C25H52,写出石蜡完全燃烧的符号表达式:C25H52+38O2$\frac{\underline{\;点燃\;}}{\;}$25CO2+26H2O.
【实验拓展】
小组同学以“研究不同高度的蜡烛哪只先熄灭”为课题设计了以下实验:
查阅资料:二氧化碳的密度比空气大
实验步骤:①点燃两支高低不同的蜡烛②用一只大烧杯同时倒扣在两支燃烧的蜡烛上,用秒表计时.③重复实验四次,实验记录如下:实验结论:分析表中数据,你得到的结论是在同样大小的倒扣的烧杯中,较高的蜡烛燃烧的时间短;
分析反思:二氧化碳的密度比空气大,为什么实验结果与我们的猜想不符呢?通过讨论,同学们一致认为原因可能是燃烧产生的二氧化碳温度较高,密度较小,不易沉降到烧杯底部,反而聚集到烧杯的上部,致使高蜡烛先熄灭.学以致用:当室内发生火灾,应用湿毛巾捂住口鼻,并伏低(填“直立”或“伏低”)身子前行寻找逃生出口.

甲组:烧杯内壁有无色液滴
乙组:烧杯内壁有无色液滴,烧杯底部附着有黑色固体
【提出问题】同学们查阅教材实验,得知无色液滴是水,
但黑色固体是什么呢?
【提出猜想】黑色固体是碳
【实验验证】利用如图2所示装置,甲,乙小组的同学分别设计了以下方案进行验证.
| 实验操作 | 实验现象 | |
| 甲组 | 取少量该黑色固体于a中,通入空气,点燃酒精灯加热. | 黑色固体燃烧,发出红光,b中溶液变浑浊. |
| 乙组 | 取少量该黑色固体于a中,通入氧气(或O2),点燃酒精灯加热. | 黑色固体剧烈燃烧,发出白光,b中溶液变浑浊. |
(1)实验结束时,停止通入气体,后续实验操作顺序应是BA(填字母序号).
A.熄灭酒精灯,停止加热 B.将试管b移走
(2)b中的实验现象说明黑色固体燃烧生成了二氧化碳,由此可推断猜想正确,理由是化学反应前后元素种类不变,二氧化碳的碳元素一定来自黑色固体.
【实验反思】
(1)进一步实验发现,罩在火焰上方的烧杯位置越低,产生黑色固体越多.查阅资料可知:蜡烛+氧气(足量)→二氧化碳+水;蜡烛+氧气(少量)→一氧化碳+水;…(反应条件均为“点燃”)由此推测乙组实验产生黑色固体的原因是烧杯位置降低使氧气的量减少,氧气的量少到一定程度时蜡烛和氧气反应产生黑色固体碳.
(2)甲、乙小组最终证明了蜡烛中一定含有C(填字母序号).
A.碳、氢和氧三种元素B.碳和氧两种元素C.碳和氢两种元素
(3)石蜡的主要成分为C25H52,写出石蜡完全燃烧的符号表达式:C25H52+38O2$\frac{\underline{\;点燃\;}}{\;}$25CO2+26H2O.
【实验拓展】
小组同学以“研究不同高度的蜡烛哪只先熄灭”为课题设计了以下实验:
查阅资料:二氧化碳的密度比空气大
实验步骤:①点燃两支高低不同的蜡烛②用一只大烧杯同时倒扣在两支燃烧的蜡烛上,用秒表计时.③重复实验四次,实验记录如下:实验结论:分析表中数据,你得到的结论是在同样大小的倒扣的烧杯中,较高的蜡烛燃烧的时间短;
| 实验次数 | 高蜡烛燃烧的时间 | 矮蜡烛燃烧的时间 |
| 第一次 | 23秒18 | 26秒06 |
| 第二次 | 23秒19 | 24秒94 |
| 第三次 | 20秒02 | 21秒45 |
| 第四次 | 15秒16 | 19秒10 |
9.在消防知识中有一个词叫做“物理性爆炸”,是指在没有发生化学反应的情况下发生的爆炸,下列各项描述中属于物理性爆炸的是( )
| A. | 煤矿中因遭到明火而发生的瓦斯爆炸 | |
| B. | 高压锅因排气孔堵塞而爆炸 | |
| C. | 节日的烟花在空中爆炸 | |
| D. | 厨房中因燃气泄漏而爆炸 |
19.区分下列各组物质的两种方法都正确的是( )
| 选项 | 需要区分的物质 | 方法一 | 方法二 |
| A | 氧化铁和氧化铜 | 看状态 | 用一氧化碳还原 |
| B | 木炭粉和铁粉 | 观察颜色 | 加稀盐酸 |
| C | 饱和硝酸钾溶液和饱和氢氧化钙溶液 | 升温观察 | 通入二氧化碳 |
| D | 氯化钠和硝酸铵 | 加适量水溶解后测温 度变化 | 观察颜色 |
| A. | A | B. | B | C. | C | D. | D |
6. 海洋为人类提供了宝贵的自然资源.
海洋为人类提供了宝贵的自然资源.
(1)食用海鱼摄取的主要营养素是蛋白质.
(2)右图为海水淡化装置,获得的蒸馏水属于B(填字母序号).
A.单质 B.化合物 C.混合物
(3)从海水中提取食盐,采用的方法是蒸发.
(4)资料:20℃时四种物质的溶解度如下:
计算:20℃时饱和食盐水溶质质量分数26.5%.
用氯化钠和碳酸氢铵(NH4HCO3)可制备碳酸氢钠和氯化铵(NH4Cl),该反应可表示为:
NaCl+NH4HCO3═NaHCO3+NH4Cl.
按上述化学方程式反应,在20℃时,饱和食盐水和饱和的碳酸氢铵溶液混合最可能产生沉淀的物质是NaHCO3; 从溶液中分离出该沉淀的操作是过滤.
 海洋为人类提供了宝贵的自然资源.
海洋为人类提供了宝贵的自然资源.(1)食用海鱼摄取的主要营养素是蛋白质.
(2)右图为海水淡化装置,获得的蒸馏水属于B(填字母序号).
A.单质 B.化合物 C.混合物
(3)从海水中提取食盐,采用的方法是蒸发.
(4)资料:20℃时四种物质的溶解度如下:
| 物质 | NaCl | NH4HCO3 | NH4Cl | NaHCO3 |
| 溶解度/g | 36.0 | 21.6 | 37.2 | 9.6 |
用氯化钠和碳酸氢铵(NH4HCO3)可制备碳酸氢钠和氯化铵(NH4Cl),该反应可表示为:
NaCl+NH4HCO3═NaHCO3+NH4Cl.
按上述化学方程式反应,在20℃时,饱和食盐水和饱和的碳酸氢铵溶液混合最可能产生沉淀的物质是NaHCO3; 从溶液中分离出该沉淀的操作是过滤.
3.石灰石是我国的主要矿产之一,为测定其中碳酸钙的含量,课外活动小组的同学称取50g石灰样品.分别在5只烧杯中进行了实验,实验数据见下表(假设每个烧杯中都充分反应,石灰石中其它成分既不溶于水,也不与水反应):
(1)表中X的值为37.36g;
(2)烧杯①②③(填序号)中反应后碳酸钙有剩余;
(3)烧杯④(填序号)中石灰石与稀盐酸恰好完全反应;
(4)求样品中碳酸钙的质量分数(写出计算过程)
| 烧杯① | 烧杯② | 烧杯③ | 烧杯④ | 烧杯⑤ | |
| 加入样品的质量/g | 10 | 10 | 10 | 10 | 10 |
| 加入稀盐酸的质量/g | 10 | 20 | 30 | 40 | 50 |
| 烧杯中剩余物质的质量/g | 19.12 | 28.24 | x | 46.48 | 56.48 |
(2)烧杯①②③(填序号)中反应后碳酸钙有剩余;
(3)烧杯④(填序号)中石灰石与稀盐酸恰好完全反应;
(4)求样品中碳酸钙的质量分数(写出计算过程)
 最近,据权威实验结果显示,我国的地表水被检测出含有68种抗生素,大部分地区水中检出的抗生素频率高达100%,水资源的安全问题再次引发民众的担忧,水和空气一样决定着我们的健康,而家用净水器在不少家庭中已成为不可缺少的滤水装置.
最近,据权威实验结果显示,我国的地表水被检测出含有68种抗生素,大部分地区水中检出的抗生素频率高达100%,水资源的安全问题再次引发民众的担忧,水和空气一样决定着我们的健康,而家用净水器在不少家庭中已成为不可缺少的滤水装置.