题目内容
16.化工生产中需要对原料提纯,以利于提高产品质量,经测定某氯化钠样品中混有硫酸钠,为了除去杂质并制得纯净的氯化钠固体,在实验室研究中某学生设计方案如下: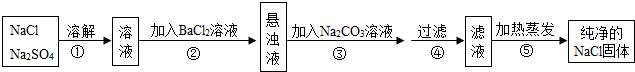
回答下列问题.
(1)过滤操作中玻璃棒的作用是引流,蒸发结晶操作中待蒸发皿中出现较多固体停止加热.
(2)操作②能否用硝酸钡溶液?说明理由不能用硝酸钡溶液,会引入新的硝酸钠杂质无法除去;进行操作②后,如何判断硫酸钠已除尽,方法是取清液少许,滴加氯化钡溶液,看是否有沉淀生成;
(3)操作③的目的是使钡离子完全沉淀,③、④操作顺序能否交换,其理由是不能,得不到滤液;此设计方案是否严密,说明理由不严密,过量的碳酸钠没有除去.
(4)实验中学化学兴趣小组为测定某石灰石样品(杂质不溶于水,也不与酸反应)中碳酸钙的质量分数,进行如图所示的实验.
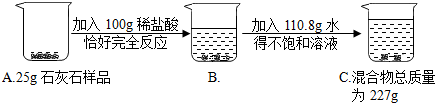
请根据以上信息计算:样品中碳酸钙的质量分数?
分析 (1)根据玻璃棒在过滤时起引流作用,蒸发操作中的注意事项进行分析;
(2)根据硝酸钡溶液和硫酸钠反应生成硫酸钡沉淀和硝酸钠,硝酸钠属于新的杂质进行解答;
根据氯化钡和硫酸溶液反应会生成硫酸钡沉淀和氯化钠进行解答;
(3)根据碳酸钠和氯化钡反应生成碳酸钡沉淀和氯化钠进行解答;
根据最后过量的碳酸钠没有除去进行解答;
(4)根据质量守恒定律,前后质量之差为生成的二氧化碳的质量,根据二氧化碳的质量可以计算出碳酸钙的质量.
解答 解:(1)过滤操作中玻璃棒的作用是引流,蒸发结晶操作中待蒸发皿中出现较多固体停止加热;
(2)硝酸钡溶液和硫酸钠反应生成硫酸钡沉淀和硝酸钠,硝酸钠属于新的杂质,所以不能用硝酸钡溶液;氯化钡和硫酸溶液反应会生成硫酸钡沉淀和氯化钠,所以判断硫酸钠已除尽,方法是向上清液中滴加氯化钡溶液,看是否有沉淀生成;
(3)碳酸钠和氯化钡反应生成碳酸钡沉淀和氯化钠,所以操作③的目的是使钡离子完全沉淀;若③、④操作顺序交换,即先过滤后加入碳酸钠溶液,过滤去硫酸钡沉淀后,加入的碳酸钠会和过量的氯化钡反应,再次产生悬浊液,若不过滤则得不到滤液,因此不能交换顺序;最后过量的碳酸钠没有除去,所以此设计方案不严密;
(4)根据质量守恒定律可知,生成CO2的质量为:25g+100g+110.8g-227g=8.8g,
设该石灰石样品中CaCO3的质量为x,
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 8.8g
$\frac{100}{x}$=$\frac{44}{8.8g}$
x=20g
样品中碳酸钙的质量分数为:$\frac{20}{25}$×100%=80%
答:样品中碳酸钙的质量分数为80%.
故答案为:(1)引流,蒸发皿中出现较多固体;
(2)不能用硝酸钡溶液,会引入新的硝酸钠杂质无法除去;取清液少许,滴加氯化钡溶液,看是否有沉淀生成;
(3)使钡离子完全沉淀;不能,得不到滤液;不严密,过量的碳酸钠没有除去;
(4)样品中碳酸钙的质量分数为80%.
点评 本题主要考查了物质的分离操作和除去杂质的方法,要根据物质的性质选择适当的方法或试剂进行解答,本题难度较大,培养学生对知识的应用和理解的能力.

| A. | FeCl3 NaOH NaCl | B. | Na2CO3 HCl BaCl2 | ||
| C. | CuSO4 KCl HCl | D. | Na2CO3 NaCl Na2CO3 |
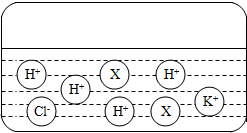 某溶液中大量存在的离子如图所示,其中X可能是( )
某溶液中大量存在的离子如图所示,其中X可能是( )| A. | Ag+ | B. | OH- | C. | CO32- | D. | SO42- |
| A. | 钠米碳虽然质地柔软 | |
| B. | 纳米氧化锌能吸收电磁波 | |
| C. | 金黄的金粉应该属于纳米材料 | |
| D. | 在空气中能自燃的铁粉应该属于纳米材料 |
| A. | 井水 | B. | 矿泉水 | C. | 硬水 | D. | 蒸馏水 |
| A. | 溶液的上层浓度小,下层浓度大 | |
| B. | 物质在溶解得到溶液的过程中,通常有放热或吸热现象出现 | |
| C. | 溶液蒸干后,均能得到固体物质 | |
| D. | 溶液中只有一种溶质时,溶液为纯净物 |
