题目内容
5. 海水晒盐后得到的晶体是粗盐,剩余的液体成为苦卤,苦卤中除氯化钠外还含有多种成分,在食品、化工等方面有重要作用,请根据已知信息回答以下问题:
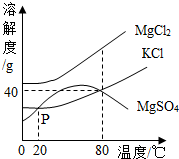
海水晒盐后得到的晶体是粗盐,剩余的液体成为苦卤,苦卤中除氯化钠外还含有多种成分,在食品、化工等方面有重要作用,请根据已知信息回答以下问题:(1)P点的含义是80℃时氯化钾和硫酸镁的溶解度相同.
(2)80℃时,MgSO4的溶解度为40g.
(3)80℃时,把40gKCl放入50g水中,所得溶液的质量为70g,此时该溶液的溶质的质量分数为28.6%.(保留一位小数)
(4)将80℃时把MgCl2、KCl、MgSO4三种物质饱和溶液的温度降到20℃时,三种溶液的溶质的质量分数的大小关系是MgCl2>KCl=MgSO4.
(5)将苦卤在80℃以上温度蒸发,首先析出的晶体应该是MgSO4.
分析 (1)根据溶解度曲线可知,P点的含义是80℃时氯化钾和硫酸镁的溶解度相同进行解答;
(2)根据溶解度曲线可知,80℃时,MgSO4的溶解度为40g进行解答;
(3)根据溶解度曲线可知,80℃时,MgSO4的溶解度为40g进行解答;
(4)根据溶解度曲线可知,20℃时MgCl2、KCl、MgSO4的溶解度大小关系为MgCl2>KCl=MgSO4进行解答;
(5)根据在80℃以上硫酸镁的溶解度最小进行解答.
解答 解:(1)根据溶解度曲线可知,P点的含义是80℃时氯化钾和硫酸镁的溶解度相同;故填:80℃时氯化钾和硫酸镁的溶解度相同;
(2)根据溶解度曲线可知,80℃时,MgSO4的溶解度为40g;故填:40;
(3)根据溶解度曲线可知,80℃时,MgSO4的溶解度为40g,即80℃时,100g水中最多溶解40g硫酸镁,所以80℃时,把40gKCl放入50g水中,最多溶解20g硫酸镁,故所得溶液的质量为20g+50g=70g,此时该溶液的溶质的质量分数=$\frac{20g}{20g+50g}×100%$=28.6%;故填:70;28.6%;
(4)根据溶解度曲线可知,20℃时MgCl2、KCl、MgSO4的溶解度大小关系为MgCl2>KCl=MgSO4,且将80℃时把MgCl2、KCl、MgSO4三种物质饱和溶液的温度降到20℃时,都会析出晶体,溶质质量分数都要减小,所以此时三种溶液的溶质的质量分数的大小关系是;故填:MgCl2>KCl=MgSO4;
(5)在80℃以上硫酸镁的溶解度最小,所以将苦卤在80℃以上温度蒸发,首先析出的晶体应该是硫酸镁.故填:MgSO4.
点评 主要考查了固体溶解度曲线的意义及温度对固体溶解度的影响,培养学生应用知识解决问题的能力.

练习册系列答案
相关题目
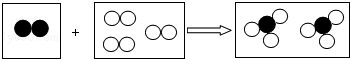
13.如图是某化学反应的微观模型,“ ”、“
”、“ ”分别表示不同元素的原子,下列各项中对图示模型理解正确的是( )
”分别表示不同元素的原子,下列各项中对图示模型理解正确的是( )
 ”、“
”、“ ”分别表示不同元素的原子,下列各项中对图示模型理解正确的是( )
”分别表示不同元素的原子,下列各项中对图示模型理解正确的是( )
| A. | 该反应属于分解反应 | |
| B. | 反应中共有两种元素参加 | |
| C. | 反应物和生成物中只有一种单质 | |
| D. | 参加反应的两种物质分子个数之比为2:3 |
11.已知一定质量的乙醇和一定是质量的氧气恰好完全反应,生成二氧化碳8.8g,一氧化碳5.6g,则该反应中生成的水的质量为( )
| A. | 3.6g | B. | 5.4g | C. | 7.2g | D. | 10.8g |
14.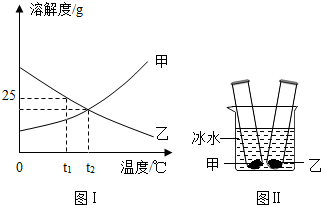 甲、乙两种固体物质的溶解度曲线如图I所示,常温下,分别向装有适量甲、乙物质的两支试管里加入等量的蒸馏水,充分振荡后,两支试管底部均有未溶解的固体;再将两支试管放入盛有冰水混合物的烧杯里,如图II所示.下列说法不正确的是( )
甲、乙两种固体物质的溶解度曲线如图I所示,常温下,分别向装有适量甲、乙物质的两支试管里加入等量的蒸馏水,充分振荡后,两支试管底部均有未溶解的固体;再将两支试管放入盛有冰水混合物的烧杯里,如图II所示.下列说法不正确的是( )
 甲、乙两种固体物质的溶解度曲线如图I所示,常温下,分别向装有适量甲、乙物质的两支试管里加入等量的蒸馏水,充分振荡后,两支试管底部均有未溶解的固体;再将两支试管放入盛有冰水混合物的烧杯里,如图II所示.下列说法不正确的是( )
甲、乙两种固体物质的溶解度曲线如图I所示,常温下,分别向装有适量甲、乙物质的两支试管里加入等量的蒸馏水,充分振荡后,两支试管底部均有未溶解的固体;再将两支试管放入盛有冰水混合物的烧杯里,如图II所示.下列说法不正确的是( )| A. | t1℃时,乙物质的饱和溶液的溶质质量分数<25% | |
| B. | t2℃时,甲物质的溶解度=乙物质的溶解度 | |
| C. | 若甲中含有少量的杂质乙,可采用蒸发结晶方法提纯甲 | |
| D. | 在图Ⅱ实验中看到的实验现象是甲试管中固体增多,乙试管里固体减少 |
 化学与生活、生产密切相关.请回答下列问题:
化学与生活、生产密切相关.请回答下列问题: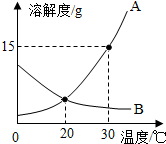 A、B两种固体物质的溶解度曲线如图所示.请回答:
A、B两种固体物质的溶解度曲线如图所示.请回答: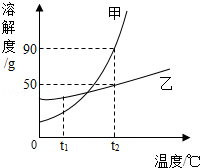 溶解度是物质溶解性的定量表示,溶解度曲线可表示物质在不同温度下的溶解度.甲、乙两种物质的溶解度曲线如图所示,根据图示回答下列问题:
溶解度是物质溶解性的定量表示,溶解度曲线可表示物质在不同温度下的溶解度.甲、乙两种物质的溶解度曲线如图所示,根据图示回答下列问题: