题目内容
15.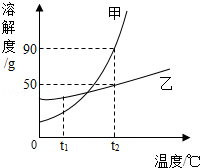 溶解度是物质溶解性的定量表示,溶解度曲线可表示物质在不同温度下的溶解度.甲、乙两种物质的溶解度曲线如图所示,根据图示回答下列问题:
溶解度是物质溶解性的定量表示,溶解度曲线可表示物质在不同温度下的溶解度.甲、乙两种物质的溶解度曲线如图所示,根据图示回答下列问题:(1)甲、乙两种物质中溶解度受温度影响较大的是甲物质.
(2)若甲物质中混有少量的乙物质,提纯甲物质最好采取的方法是
降温结晶(填“降温结晶”或“蒸发结晶”).
(3)t2℃时,乙物质的溶解度为50 g;t2℃时,若将30g乙物质
加入到50g水中,所得溶液的溶质质量分数是33.3%(计算结果精确到0.1%).
(4)将t1℃的甲、乙两物质的饱和溶液(均无固体物质剩余)升温到t2℃时,所得甲物质溶液的溶质质量分数小于乙物质溶液的溶质质量分数(填“大于”“小于”“等于”之一).
分析 (1)根据物质的溶解度曲线可以判断物质的溶解度受温度变化的影响情况;
(2)从溶液中结晶的方法有两种:蒸发结晶和降温结晶,物质的溶解度受温度变化影响较小时,应该用蒸发结晶;物质的溶解度受温度变化影响较大时,应该用降温结晶;
(3)根据物质的溶解度曲线可以判断某一温度时物质的溶解度大小;
根据物质的溶解度曲线、溶质质量、溶剂质量可以计算溶质质量分数;
(4)饱和溶液的溶质质量分数=$\frac{溶解度}{100g+溶解度}$×100%.
解答 解:(1)由物质的溶解度曲线可知,甲、乙两种物质中溶解度受温度影响较大的是甲物质.
故填:甲.
(2)由物质的溶解度曲线可知,甲物质的溶解度受温度变化影响较大,乙物质的溶解度受温度变化影响较小,若甲物质中混有少量的乙物质,提纯甲物质最好采取的方法是降温结晶.
故填:降温结晶.
(3)由物质的溶解度曲线可知,t2℃时,乙物质的溶解度为50g;
t2℃时,若将30g乙物质加入到50g水中,只能够溶解25g,所得溶液的溶质质量分数为:$\frac{25g}{25g+50g}$×100%=33.3%.
故填:50;33.3%.
(4)t1℃时,乙的溶解度大于甲的溶解度,即t1℃时甲的饱和溶液的质量分数小于乙的饱和溶液的质量分数,t1℃的甲、乙两物质的饱和溶液升温到t2℃时,溶质和溶剂质量都不变,因此所得甲物质溶液的溶质质量分数小于乙物质溶液的溶质质量分数.
故填:小于.
点评 溶解度曲线能定量地表示出溶解度变化的规律,从溶解度曲线可以看出:同一溶质在不同温度下的溶解度不同;同一温度下,不同溶质的溶解度可能相同,也可能不同;温度对不同物质的溶解度影响不同.

练习册系列答案
 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案
相关题目
6.埃博拉病毒是当今世界上最凶险的病毒之一,其致死率可高达90%,日本最近研制出抗击埃博拉病毒的药物Favipiravir,其化学式为C5H4N3O2F,下列有关这种药物的说法错误的是( )
| A. | 它由五种元素组成 | B. | 它的分子中氢、氧原子个数比为2:1 | ||
| C. | 该药物由15个原子构成 | D. | 该药物中碳元素的质量分数最大 |
10.下列关于相应微粒的描述中,不正确的是( )
| A. | 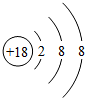 化学性质稳定 | B. | 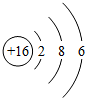 易形成阴离子 | C. | 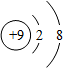 带正电荷 | D. | 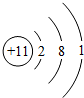 易失电子 |
7.正确观察和描述实验现象是学好化学的因素之一,下列说法中不正确的是( )
| A. | 镁条在空气中燃烧,发出耀眼的白光 | |
| B. | 硫在氧气中燃烧,发出明亮的蓝紫色火焰 | |
| C. | 一氧化碳在在空气中燃烧发出淡蓝色火焰 | |
| D. | 细铁丝在氧气中燃烧,火星四射,有黑色固体生成 |
4.下列说法错误的是( )
| A. | 水基型灭火器可用来扑灭由汽油、柴油等可燃性液体引起的失火 | |
| B. | KNO3的不饱和溶液变为饱和溶液,其溶液的溶质质量分数一定变大 | |
| C. | 水净化程度由低到高的顺序是静置、过滤、吸附、蒸馏 | |
| D. | 碱一定含有氧元素,盐不一定含有氧元素 |
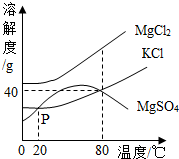 海水晒盐后得到的晶体是粗盐,剩余的液体成为苦卤,苦卤中除氯化钠外还含有多种成分,在食品、化工等方面有重要作用,请根据已知信息回答以下问题:
海水晒盐后得到的晶体是粗盐,剩余的液体成为苦卤,苦卤中除氯化钠外还含有多种成分,在食品、化工等方面有重要作用,请根据已知信息回答以下问题:
