题目内容
19.实验室中有一瓶含有少量氯化钠和可溶性杂质的硫酸钠样品.某化学兴趣小组对该样品成分进行定量测定,甲、乙、丙三位同学分别称取一定质量的样品放入烧杯中,溶入足量水后过滤得到滤液;再向滤液中加入一定质量的氯化钡溶液,充分反应后过滤,将沉淀洗涤、干燥并称量.相关实验数据记录如下:(Na2SO4+BaCl2═BaSO4↓+2NaCl)| 称量项目 | 甲 | 乙 | 丙 |
| 所取样品的质量/g | 15 | 15 | 20 |
| 加入氯化钡溶液的质量/g | 150 | 100 | 100 |
| 反应后所得沉淀的质量/g | 23.3 | 23.3 | 23.3 |
(1)乙同学(选填“甲”“乙”或“丙”)所取用的样品与氯化钡溶液恰好完全反应.
(2)计算该样品中硫酸钠的质量分数.(写出计算步骤,计算结果保留到0.1%)
(3)若欲计算出样品与氯化钡溶液恰好完全反应时所得溶液的溶质质量分数,上述实验过程中还需要测定的数据是水的质量.
分析 (1)根据甲、乙比较,100g氯化钡完全反应,乙、丙比较,15g样品完全反应进行分析;
(2)根据氯化钡和硫酸钠反应会生成硫酸钡沉淀和氯化钠,然后结合题中的数据进行分析;
(3)根据计算质量分数需要知道溶液质量和溶质质量进行分析.
解答 解:(1)甲、乙比较,100g氯化钡完全反应,乙、丙比较,15g样品完全反应,所以乙同学所取用的样品与氯化钡溶液恰好完全反应;
(2)设参加反应的硫酸钠为x,
Na2SO4+BaCl2=BaSO4↓+2NaCl
142 233
x 23.3g
$\frac{142}{x}=\frac{233}{23.3g}$
x=14.2g
所以样品中硫酸钠的质量分数为:$\frac{14.2g}{15g}$×100%=94.7%;
(3)计算质量分数需要知道溶液质量和溶质质量,溶质质量通过化学方程式可以求出生成的氯化钠和硫酸钠,然后求出样品中的氯化钠;溶液质量需要应用质量守恒定律,反应物的质量减去沉淀的质量即可,但是反应物不知道水的质量,所以还需要测定的数据是水的质量.
故答案为:(1)乙;(2)94.7%;(3)水的质量.
点评 本题的难度不大,根据化学反应方程式的计算步骤和格式进行计算即可.

练习册系列答案
 提分百分百检测卷系列答案
提分百分百检测卷系列答案 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案
相关题目
10.某化学兴趣小组在化学实验室发现一瓶没有标签的淡黄色粉末,同学们对探究该粉末产生浓厚兴趣,并在老师的指导下进行探究活动.
【提出问题】这种淡黄色粉末是什么?有什么性质和用途?
【查阅资料】①硫是一种、淡黄色粉末,不溶于水且不与水反应;
②过氧化钠(Na2O2)是淡黄色粉末,在常温下能与水反应生成极易容于水的氢氧化钠和一种无色无味的气体;
③过氧化钠在常温下能与二氧化碳反应生成碳酸钠和氧气,其符号表达式为:CO2+Na2O2→Na2CO3+O2.过氧化钠在呼吸面具中和潜水艇里常用作供氧剂.
【猜想与探究】
①猜想:淡黄色粉末可能是:a.硫;b.过氧化钠;c.硫和过氧化钠的混合物.
②猜想:过氧化钠与水反应生成的气体可能是:a.O2;b.H2.作出这样猜想的依据是反应物中有H、O 或化学反应前后元素种类保持不变.
【交流与讨论】
1.与我们学过的制氧气方法相比,常选用过氧化钠作为呼吸面具和潜水艇的供氧剂的主要理由是:消耗二氧化碳,产生氧气.
2.下列关于Na2O2说法不正确的是ac(填字母序号).
a.Na2O2中氧元素的化合价是-2价
b.Na2O2必须密封保存
c.Na2O2可以用来除去二氧化碳中的水蒸气.
【提出问题】这种淡黄色粉末是什么?有什么性质和用途?
【查阅资料】①硫是一种、淡黄色粉末,不溶于水且不与水反应;
②过氧化钠(Na2O2)是淡黄色粉末,在常温下能与水反应生成极易容于水的氢氧化钠和一种无色无味的气体;
③过氧化钠在常温下能与二氧化碳反应生成碳酸钠和氧气,其符号表达式为:CO2+Na2O2→Na2CO3+O2.过氧化钠在呼吸面具中和潜水艇里常用作供氧剂.
【猜想与探究】
①猜想:淡黄色粉末可能是:a.硫;b.过氧化钠;c.硫和过氧化钠的混合物.
| 探究 | 实验操作 | 实验现象 | 实验结论 |
| ①在一支洁净的试管中加入适量的上述淡黄色粉末,再加入足量的蒸馏水 | 有气泡冒出,固体全部消失 | 猜想b成立. (填字母序号) |
| 继续探究 | 实验操作 | 实验现象 | 实验结论 |
| ②在试管中加入适量的该淡黄色粉末和蒸馏水,将带火星的木条(或燃着的木条)放在试管口部. | 木条复燃 | 生成的气体是 O2 |
1.与我们学过的制氧气方法相比,常选用过氧化钠作为呼吸面具和潜水艇的供氧剂的主要理由是:消耗二氧化碳,产生氧气.
2.下列关于Na2O2说法不正确的是ac(填字母序号).
a.Na2O2中氧元素的化合价是-2价
b.Na2O2必须密封保存
c.Na2O2可以用来除去二氧化碳中的水蒸气.
7.下列有关质量守恒定律的认识,正确的是( )
| A. | 通过化学变化,既能改变物质的种类,也能改变参加反应的物质的总质量 | |
| B. | 质量守恒定律揭示了化学变化中宏观物质之间的质量关系,与微观过程无关 | |
| C. | 蜡烛燃烧后质量减小,说明质量守恒定律不是普遍规律 | |
| D. | 任何化学变化都遵守质量守恒定律 |
11.下列对物质在氧气中燃烧的现象和所属反应类型描述正确的是(
| A. | 铁--黄色火焰--化合反应 | B. | 红磷--蓝色火焰--化合反应 | ||
| C. | 碳--明亮白光--化合反应 | D. | 蜡烛--黄色火焰--分解反应 |
8.关于原子的说法错误的是( )
| A. | 原子是化学变化中的最小粒子 | |
| B. | 元素的原子序数等于原子的核电荷数 | |
| C. | 元素的化学性质取决于原子核内的质子数 | |
| D. | 在物质发生化学变化时,原子的种类不变,元素也不会改变 |
 现有甲、乙、丙、丁四种物质,它们均含有同一种元素,该元素在地壳中的含量位列第一,其中甲为黑色固体氧化物,乙是造成温室效应的主要物质,丙为单质,它们之间的关系如图所示(图中“-”表示两端的物质能反应,“→”表示转化关系,反应条件、部分生成物已略去).
现有甲、乙、丙、丁四种物质,它们均含有同一种元素,该元素在地壳中的含量位列第一,其中甲为黑色固体氧化物,乙是造成温室效应的主要物质,丙为单质,它们之间的关系如图所示(图中“-”表示两端的物质能反应,“→”表示转化关系,反应条件、部分生成物已略去).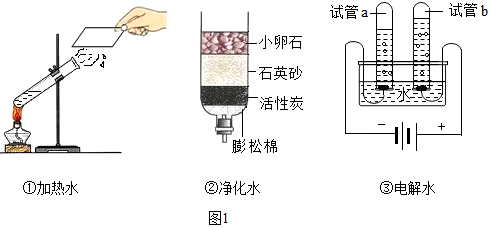
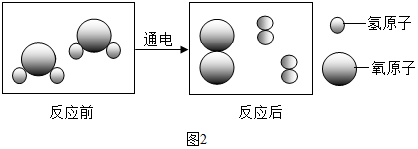
 如图是“尾气催化转换器”将汽车尾气中有毒气体转变为无毒气体的微观示意图,其中不同的圆球代表不同原子.下列说法正确的是B
如图是“尾气催化转换器”将汽车尾气中有毒气体转变为无毒气体的微观示意图,其中不同的圆球代表不同原子.下列说法正确的是B