题目内容
1.下列变化中与其他三种不同的是( )| A. | 食物腐败 | B. | 水在通直流电情况下分解 | ||
| C. | 白磷自燃 | D. | 分离液态空气制氧气 |
分析 化学变化是指有新物质生成的变化,物理变化是指没有新物质生成的变化,化学变化和物理变化的本质区别是否有新物质生成;据此分析判断.
解答 解:A、食物腐败过程中有新物质生成,属于化学变化.
B、水在通直流电情况下分解过程中有新物质氢气等生成,属于化学变化.
C、白磷自燃过程中有新物质生成,属于化学变化.
D、分离液态空气制氧气过程中没有新物质生成,属于物理变化.
故选D.
点评 本题难度不大,解答时要分析变化过程中是否有新物质生成,若没有新物质生成属于物理变化,若有新物质生成属于化学变化.

练习册系列答案
 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案
相关题目
11.下列化学用语与所表述的意义相符的是( )
| A. | 2Ca2+:带2个单位正电荷的钙离子 | B. | O2:2个氧原子 | ||
| C. | $\stackrel{0}{N}$2:氮元素的化合价为0 | D. | 2H2O:2个水分子 |
9.下列化学方程式及其对应的基本反应类型正确的是( )
| A. | CaCO3+2HCl═CaCl2+H2O+CO2↑--化合反应 | |
| B. | 2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑--分解反应 | |
| C. | Ca+2H2O═Ca(OH)2+H2↑--化合反应 | |
| D. | 2KClO3+MnO2$\frac{\underline{\;\;△\;\;}}{\;}$2KCl+MnO2+3O2↑--复分解反应 |
16.下列说法中错误的是( )
| A. | 分子可以分成原子,原子不能再分 | |
| B. | 由分子构成的物质,分子是保持物质化学性质的最小粒子 | |
| C. | 带电的粒子不一定是离子 | |
| D. | 质子数相同的粒子不一定属于同种元素 |
6.下列有关实验现象的描述正确的是( )
| A. | 铁丝在空气中被点燃,火星四射 | |
| B. | 石蜡在氧气中燃烧时,有水和二氧化碳生成 | |
| C. | 点燃纯净的氢气,会发生爆炸 | |
| D. | 硫在氧气中燃烧发出明亮的蓝紫色火焰 |
17.某化学兴趣小组对课本介绍的三种金属Mg、Ti(钛)、Cu的金属活动性进行探究.
[提出假设]a:Ti金属活动性比镁强,b:Mg金属活动性比Cu强
[查阅资料]在相同条件下,金属与酸反应,产生气泡的速度越快,则该金属活动性越强.
[实验设计]同温下,取质量相同的这三种金属薄片,分别投入等体积等浓度的足量的稀盐酸中反应,观察现象.
[回答问题](1)三种金属加入盐酸前都先用砂布将表片擦亮,其目的是A.
A.除去氧化膜,利于直接反应 B.使表面不平整,易反应
C.使表面光亮,易观察现象 D.使反应温度相同,易反应
(2)填写下表中的有关现象和结论:
(3)探究结束后,小涛同学说我还有其它办法也能得出三种金属在金属活动顺序中的相对位置关系,他选用了三种药品进行实验,则他选用的三种药品可能是Mg、TiSO4 、Cu.
[总结与归纳]由上述试验得出比较金属活动性强弱的方法有:
①通过金属与酸反应比较;②通过金属与盐溶液反应比较.
[提出假设]a:Ti金属活动性比镁强,b:Mg金属活动性比Cu强
[查阅资料]在相同条件下,金属与酸反应,产生气泡的速度越快,则该金属活动性越强.
[实验设计]同温下,取质量相同的这三种金属薄片,分别投入等体积等浓度的足量的稀盐酸中反应,观察现象.
[回答问题](1)三种金属加入盐酸前都先用砂布将表片擦亮,其目的是A.
A.除去氧化膜,利于直接反应 B.使表面不平整,易反应
C.使表面光亮,易观察现象 D.使反应温度相同,易反应
(2)填写下表中的有关现象和结论:
| Ti | Mg | Cu | |
| 与盐酸反应现象 | 放出气泡速度缓慢 | 放出气泡速度快 | 无现象 |
| 结论 | 原假设中a不正确(填“a”、“b”、“a b”)理由是钛与盐酸反应放出气泡速度缓慢,镁与盐酸反应放出气泡速度快;三种金属的活动性顺序为Mg>Ti>Cu. | ||
[总结与归纳]由上述试验得出比较金属活动性强弱的方法有:
①通过金属与酸反应比较;②通过金属与盐溶液反应比较.
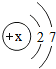 ,该元素的核电数x为9,它的原子在化学反应中容易得到1个电子.
,该元素的核电数x为9,它的原子在化学反应中容易得到1个电子.