题目内容
 某探究性学习小组,利用下列改进装置对物质燃烧的条件进行探究.
某探究性学习小组,利用下列改进装置对物质燃烧的条件进行探究.【查阅资料】
①白磷有剧毒,可以用酸性高锰酸钾溶液除去白磷.
②五氧化二磷扩散到空气中,刺激人的呼吸道,影响健康、污染环境.
(1)打开止水夹,缓缓推动注射器活塞,观察到烧瓶中白磷周围产生火星.液面上方产生大量白烟.该现象说明过氧化钠能与水反应生成
(2)此实验充分体现了绿色化学的要求,对有害物质进行了处理.氢氧化钠的作用是
(3)小组成员对过氧化钠(Na2O2)与水反应生成的另一种物质是什么进行了以下探究:
【猜想】
猜想一:氢氧化钠 猜想二:碳酸钠
经过大家讨论,猜想二不成立,原因是
对于猜想一是否成立,同学们进行了如下实验:
【实验论证】
| 实验操作 | 实验现象 | 实验结论 |
| 取少量过氧化钠固体于试管中,加足量水,并向其中滴入少量 | 猜想一成立 |
过氧化钠与水反应的化学方程式为
【拓展延伸】
过氧化钠是一种黄色固体,还会与二氧化碳反应生成碳酸钠和氧气,潜水艇中常利用该反应来提供氧气.判断一瓶空气中长久放置的过氧化钠是否变质的方法是
考点:燃烧的条件与灭火原理探究,气体的净化(除杂),碱的化学性质,书写化学方程式、文字表达式、电离方程式
专题:科学探究
分析:(1)根据过氧化钠能与水反应生成氧气,同时证明了燃烧的条件之一是与氧气接触解答;可从资料中查阅的五氧化二磷的性质得知,它有毒,所以要从防止污染的角度来分析图1
(2)可从资料中查阅的五氧化二磷的性质得知,它有毒,所以要从防止污染的角度来分析氢氧化钠的作用;实验结束后为了处理掉残留的少量白磷,可以把氢氧化钠溶液换成酸性高锰酸钾溶液,然后向外拉注射器活塞通过大气压就高锰酸钾溶液压入烧瓶中.
(3)
【猜想】
探究生成的物质要根据质量守恒定律,化学反应前后元素的种类不变据此分析即可;
【实验论证】
根据酚酞遇碱性物质能变红解答;
【结果表达】
根据实验可知过氧化钠与水反应会生成氢氧化钠和氧气;
【拓展延伸】
根据常温下过氧化钠固体与二氧化碳反应生成碳酸钠和氧气解答.
(2)可从资料中查阅的五氧化二磷的性质得知,它有毒,所以要从防止污染的角度来分析氢氧化钠的作用;实验结束后为了处理掉残留的少量白磷,可以把氢氧化钠溶液换成酸性高锰酸钾溶液,然后向外拉注射器活塞通过大气压就高锰酸钾溶液压入烧瓶中.
(3)
【猜想】
探究生成的物质要根据质量守恒定律,化学反应前后元素的种类不变据此分析即可;
【实验论证】
根据酚酞遇碱性物质能变红解答;
【结果表达】
根据实验可知过氧化钠与水反应会生成氢氧化钠和氧气;
【拓展延伸】
根据常温下过氧化钠固体与二氧化碳反应生成碳酸钠和氧气解答.
解答:解:
(1)白磷周围产生火星.液面上方产生大量白烟,说明有氧气产生,同时证明了燃烧的条件之一是与氧气接触;
(2)氢氧化钠的作用是吸收P2O5;实验结束后为了处理掉残留的少量白磷,可以把氢氧化钠溶液换成酸性高锰酸钾溶液,然后向外拉注射器活塞通过大气压就高锰酸钾溶液压入烧瓶中.
(3)
【猜想】
参加反应的物质为Na2O2和H2O,分析其元素组成,只有Na、H、O三种元素,根据质量守恒定律,生成物也应该含有这三种元素,所以生成的另一种物质只能是氢氧化钠,不可能是Na2CO3;
【实验论证】
酚酞遇碱性溶液会变红,现在向反应后的溶液中滴入无色酚酞试液,发现酚酞试液变红色,说明反应后所得的溶液呈碱性;
【结果表达】
根据实验结果,反应后生成的物质为氢氧化钠和氧气,方程式为:2Na2O2+2H2O═4NaOH+O2↑;
【拓展延伸】
常温下过氧化钠固体与二氧化碳反应生成碳酸钠和氧气,判断一瓶空气中长久放置的过氧化钠是否变质的方法是加入稀盐酸,如果产生气泡,则证明变质.
答案:
(1)氧气;与氧气接触
(2)吸收P2O5;向外拉注射器活塞
(3)
【猜想】
反应物质中没有碳元素.
【实验论证】
【结果表达】
2Na2O2+2H2O═4NaOH+O2 ↑
【拓展延伸】
加入稀盐酸,如果产生气泡,则证明变质.
(1)白磷周围产生火星.液面上方产生大量白烟,说明有氧气产生,同时证明了燃烧的条件之一是与氧气接触;
(2)氢氧化钠的作用是吸收P2O5;实验结束后为了处理掉残留的少量白磷,可以把氢氧化钠溶液换成酸性高锰酸钾溶液,然后向外拉注射器活塞通过大气压就高锰酸钾溶液压入烧瓶中.
(3)
【猜想】
参加反应的物质为Na2O2和H2O,分析其元素组成,只有Na、H、O三种元素,根据质量守恒定律,生成物也应该含有这三种元素,所以生成的另一种物质只能是氢氧化钠,不可能是Na2CO3;
【实验论证】
酚酞遇碱性溶液会变红,现在向反应后的溶液中滴入无色酚酞试液,发现酚酞试液变红色,说明反应后所得的溶液呈碱性;
【结果表达】
根据实验结果,反应后生成的物质为氢氧化钠和氧气,方程式为:2Na2O2+2H2O═4NaOH+O2↑;
【拓展延伸】
常温下过氧化钠固体与二氧化碳反应生成碳酸钠和氧气,判断一瓶空气中长久放置的过氧化钠是否变质的方法是加入稀盐酸,如果产生气泡,则证明变质.
答案:
(1)氧气;与氧气接触
(2)吸收P2O5;向外拉注射器活塞
(3)
【猜想】
反应物质中没有碳元素.
【实验论证】
| 实验操作 | 实验现象 | 实验结论 |
| 取少量过氧化钠固体于试管中,加足量水,并向其中滴入少量 无色酚酞试液. | 酚酞试液变红色 | 猜想一成立 |
2Na2O2+2H2O═4NaOH+O2 ↑
【拓展延伸】
加入稀盐酸,如果产生气泡,则证明变质.
点评:对于装置优越性的改进一般要考虑到操作的简便性,气密性良好,反应易操控,环境保护等方面.根据已有知识,在情景相似的情况下,进行知识地大胆迁移,是解决新问题的一种重要方法,推测生成物质的化学式时,要根据质量守恒定律.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
用数轴表示某些化学知识直观、简明、易记.下列数轴表示错误的是( )
A、 三种金属活动性强弱顺序 |
B、 根据铁合金中的含碳量,将其分成生铁和钢 |
C、 生活中常见物质形成溶液的pH |
D、 空气中三种主要成分的体积分数大小 |
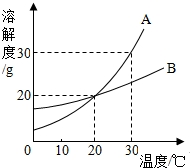 A、B两固体物质的溶解度曲线如图所示:
A、B两固体物质的溶解度曲线如图所示: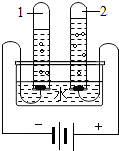 水是一种重要的自然资源,是生活、生产必不可少的物质.请回答下列问题:
水是一种重要的自然资源,是生活、生产必不可少的物质.请回答下列问题:

 如图所示为①硝酸钾、②氯化钠、③硼酸(H3BO3)的溶解度曲线图.由图可知:
如图所示为①硝酸钾、②氯化钠、③硼酸(H3BO3)的溶解度曲线图.由图可知: 如图是A,B的溶解性曲线.将t1℃时的A,B的饱和溶液(溶液底部均没有剩余晶体)升温至t2℃时,此时两种溶液的溶质质量分数大小是A
如图是A,B的溶解性曲线.将t1℃时的A,B的饱和溶液(溶液底部均没有剩余晶体)升温至t2℃时,此时两种溶液的溶质质量分数大小是A