题目内容
3.根据表中内容回答下列问题.| 温度/℃ 溶解度/g 物质 | 0 | 20 | 40 | 60 | 80 |
| KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 |
| NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 |
| Ca(OH)2 | 0.173 | 0.165 | 0.121 | 0.116 | 0.094 |
(2)根据上表推断硝酸钾与氯化钠溶解度相等时的温度范围是大于20℃小于40℃.
(3)取KNO3、NaCl两种固体各36g分别放入20℃时的100g水中充分溶解,20℃时有如图1所示的实验现象,烧杯b中溶解的物质氯化钠.
(4)如图2所示,若向烧杯中加入足量的硝酸铵使之充分溶解,可观察到的现象是烧杯内水温下降,试管中有晶体析出.

(5)如图2所示,若向试管中加入少量的硝酸钾固体,再向烧杯中加入足量的生石灰,可观察到的现象是烧杯内浑浊,水温上升,试管内固体逐渐溶解.
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:(1)通过分析溶解度表可知,随温度升高,硝酸钾溶解度的变化趋势是增大;
(2)根据上表推断硝酸钾与氯化钠溶解度相等时的温度范围是大于20℃小于40℃;
(3)20℃时,氯化钠的溶解度大于硝酸钾的溶解度,所以取KNO3、NaCl两种固体各36g分别放入20℃时的100g水中充分溶解,20℃时有如图1所示的实验现象,烧杯b中溶解的物质氯化钠;
(4)硝酸铵溶于水,溶液温度降低,所以向烧杯中加入足量的硝酸铵使之充分溶解,可观察到的现象是:烧杯内水温下降,试管中有晶体析出;
(5)氧化钙和水反应生成氢氧化钙,放出热量,所以向试管中加入少量的硝酸钾固体,再向烧杯中加入足量的生石灰,可观察到的现象是:烧杯内浑浊,水温上升,试管内固体逐渐溶解.
故答案为:(1)增大;
(2)大于20℃小于40℃;
(3)NaCl.
(4)烧杯内水温下降,试管中有晶体析出;
(5)烧杯内浑浊,水温上升,试管内固体逐渐溶解.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
 小学教材全测系列答案
小学教材全测系列答案
相关题目
14.如图四个图象中不能正确反应其对应实验操作的是( )
| A. |  向等质量的铝粉和镁粉中分别滴入质量分数相同的足量的稀盐酸 | |
| B. |  向一定量的氢氧化钡溶液中不断加入稀硫酸 | |
| C. |  等质量的块状石灰石和粉末状石灰石分别与质量分数相同的足量的稀盐酸反应 | |
| D. |  高温煅烧大理石 |
11.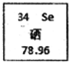 元素周期表中关于硒元素的信息如图,下列关于硒元素的说法错误的是( )
元素周期表中关于硒元素的信息如图,下列关于硒元素的说法错误的是( )
 元素周期表中关于硒元素的信息如图,下列关于硒元素的说法错误的是( )
元素周期表中关于硒元素的信息如图,下列关于硒元素的说法错误的是( )| A. | 是人体必需的微量元素 | B. | 原子核内质子数为34 | ||
| C. | 原子核内中子数为34 | D. | 相对原子质量为78.96 |
15.2015年10月,科学家屠哟哟因发现青蒿素(C15H22O5)而获得诺贝尔医学奖,它是青蒿的提取物,能溶于酒精、乙醚和石油醚,在水中几乎不溶,其中含有的过氧基团是抗疟作用的最重要结构,过氧基团易受湿、热和还原性物质的影响而被破坏,下列关于青蒿素的说法正确的是( )
| A. | 青蒿素由15个碳原子、22个氢原子和5个氧原子构成的一种有机化合物 | |
| B. | 疟疾是一种以吸血昆虫疟较为传播媒介的接触传染病 | |
| C. | 用乙醚提取青蒿素利用了青蒿素的化学性质 | |
| D. | 制药过程应在低温无水的环境中进行 |
12.初三(1)班的小朱人称“小马虎”,下面是从他的笔记中摘录的部分化学用语,你认为正确的是( )
| A. | 碳酸钠:NaCO3 | B. | 水:H2O | ||
| C. | 3个亚铁离子:3Fe3+ | D. | 两个氢原子:H2 |
13.下列物质中,由离子构成的是( )
| A. | 氯化钠 | B. | 二氧化碳 | C. | 铜 | D. | 石墨 |
 实验室利用如图实验装置进行有关化学实验,回答下列问题:
实验室利用如图实验装置进行有关化学实验,回答下列问题: