题目内容
15.某同学对含有泥沙的粗盐进行提纯,并用提纯后的氯化钠配制100g质量分数为5%的氯化钠溶液.请回答有关问题:(1)按下面的步骤提纯粗盐:
①取一定质量的粗盐样品,加水溶解;
②通过过滤操作将泥沙除去;
③将滤液移入蒸发皿,蒸发结晶,得到氯化钠晶体.
(2)在上述实验步骤中,都使用了同一仪器玻璃棒(填名称),它在步骤①和③的操作方法相同,但目的不同,步骤①的目的是搅拌,步骤③的目的是搅拌,防止滤液飞溅;
(3)利用上述实验得到的氯化钠晶体,配制100g质量分数5%的氯化钠溶液:
①配制溶液的步骤:计算、溶解、装瓶;
②量取所需的水应选用100mL的量筒.
分析 (1)粗盐的主要成分是氯化钠,根据氯化钠易溶于水、泥沙等杂质难溶于水,进行分析解答;
(2)根据溶解、过滤、蒸发操作所需的仪器,进行分析解答;
(3)①根据配制溶质质量分数一定的溶液的基本步骤进行分析解答;
②利用溶质质量=溶液质量×溶质的质量分数,溶剂质量=溶液质量-溶质质量,根据溶液的质量和溶质的质量分数,计算配制溶液所需要的水的质量;进而由所需水的体积判断所需量筒的量程.
解答 解:(1)粗盐的主要成分是氯化钠,氯化钠易溶于水、泥沙等杂质难溶于水,取一定质量的粗盐样品,加水溶解,使不溶物与食盐初步分离→过滤(把泥沙除去)→将滤液移入蒸发皿,蒸发结晶,得到氯化钠晶体蒸发;
(2)溶解、过滤、蒸发操作中都要用到的实验仪器是玻璃棒,它在步骤①溶解和③蒸发的操作方法相同,但目的不同,①溶解中作用是搅拌,加快食盐的溶解速率,③蒸发的作用是搅拌,防止滤液飞溅;
(3)①配制100g质量分数为5%的氯化钠溶液,首先计算配制溶液所需氯化钠和水的质量,再称量所需的氯化钠和量取水,最后进行溶解、装瓶;
②溶质质量=溶液质量×溶质的质量分数,配制100g质量分数为5%的氯化钠溶液,需氯化钠的质量=100g×5%=5g;溶剂质量=溶液质量-溶质质量,则所需水的质量=100g-5g=95g(合95mL),应选用100mL的量筒.
故答案为:(1)过滤;
(2)玻璃棒;搅拌,防止滤液飞溅;
(3))①称量;
②100.
点评 本题难度不大,掌握粗盐提纯的原理、实验步骤(溶解、过滤、蒸发)、所需的仪器、配制溶质质量分数一定的溶液的基本步骤等是正确解答本题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.下列知识整理的内容有错误的一组是( )
| A、性质决定用途 | B、性质不同的原因 |
| 金刚石天然最硬:划玻璃 石墨能导电:做电极,电刷 活性炭有吸附性:吸附毒气 | 金刚石与石墨:碳原子排列方式不同 CO 与 CO2:分子构成不同 |
| C、气体的比较 | D、问题解决方案 |
| 氧气:能使带火星的木条复燃 二氧化碳:能使澄清的石灰水变浑浊 一氧化碳:能使人中毒 | 温室效应:开发使用清洁能源 大气污染:积极植树造林,种草 防一氧化碳中毒:煤炉上放一壶水 |
| A. | A | B. | B | C. | C | D. | D |
6. 分类法是学习化学的重要思想方法.
分类法是学习化学的重要思想方法.
(1)人们可以对物质从不同的角度进行分类.请根据示例将酒精、醋酸、水、食盐四种物质进行分类,
并写出分类依据.
(2)某同学从物质类别的角度构建了如“图一”所示的知识网络图,借助网络图回答:
①写出用酸和碱生成氯化钠的化学方程式NaOH+HCl=NaCl+H2O.
②请把如图中①处补充完整,要求不能与图中已有信息重复.则①处应填写的内容是盐+金属.
③铁的金属活动性比铜强(选填:“强”或“弱”).可证明该结论的化学方程式是Fe+CuSO4=FeSO4+Cu.
 分类法是学习化学的重要思想方法.
分类法是学习化学的重要思想方法.(1)人们可以对物质从不同的角度进行分类.请根据示例将酒精、醋酸、水、食盐四种物质进行分类,
并写出分类依据.
| 不同类的物质 | 分类依据 | |
| 示例 | 水 | 水是氧化物,其余不是氧化物 |
| 分类一 | 食盐 | 常温下食盐是固体,其余是液体 |
| 分类二 | 醋酸 | 醋酸是酸,其余的不是酸 |
①写出用酸和碱生成氯化钠的化学方程式NaOH+HCl=NaCl+H2O.
②请把如图中①处补充完整,要求不能与图中已有信息重复.则①处应填写的内容是盐+金属.
③铁的金属活动性比铜强(选填:“强”或“弱”).可证明该结论的化学方程式是Fe+CuSO4=FeSO4+Cu.
3.去年中俄签署了东线天然气合作协议.天然气不充分燃烧时会产生炭黑或一氧化碳.
(1)CO具有还原性,写出其在工业上的一种具体用途作燃料.
(2)CO2一定条件下可以转化为CO.CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO(用化学方程式表示).
(3)将CO2通入紫色石蕊溶液中,溶液变红的原因是二氧化碳与水反应生成碳酸,碳酸能使紫色石蕊溶液变红.
(4)从表中数据分析,与煤相比,用天然气作燃料的优点有同质量煤和天然气燃烧,天然气放出热量更多.
(1)CO具有还原性,写出其在工业上的一种具体用途作燃料.
(2)CO2一定条件下可以转化为CO.CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO(用化学方程式表示).
(3)将CO2通入紫色石蕊溶液中,溶液变红的原因是二氧化碳与水反应生成碳酸,碳酸能使紫色石蕊溶液变红.
(4)从表中数据分析,与煤相比,用天然气作燃料的优点有同质量煤和天然气燃烧,天然气放出热量更多.
| 1g物质完全燃烧 | ||
| 产生二氧化碳的质量/g | 放出的热量/kJ | |
| 甲烷 | 2.75 | 56 |
| 碳 | 3.67 | 32 |
10.下列实验操作正确的是( )
| A. |  倾倒液体 | B. |  过滤 | ||
| C. |  检查气密性 | D. |  检验氧气是否收集满 |
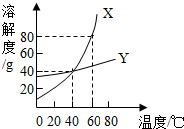 X、Y两种固体物质的溶解度曲线如图所示.回答下列问题:
X、Y两种固体物质的溶解度曲线如图所示.回答下列问题: