题目内容
4. 水是生命之源,也是一种重要的资源,日常生活、工农业生产和科学实验都离不开水,请回答下列问题:
水是生命之源,也是一种重要的资源,日常生活、工农业生产和科学实验都离不开水,请回答下列问题:(1)自然界的水一般都不是纯净物(填“纯净物”或“混合物”)含有较多可溶性钙、镁化合物的水叫硬水,生活中一般采用加热煮沸的方法把硬水转化为软水.
(2)为了除去粗盐中的Ca2+、Mg2+、SO42-等,可将粗盐溶于水,再进行如下操作:①加入适量稀盐酸 ②加入过量NaOH溶液 ③加入过量Na2CO3溶液 ④加入过量BaCl2溶液 ⑤过滤 ⑥蒸发结晶,请将上述操作按合理顺序补充完整:②④③⑤①⑥(填序号)
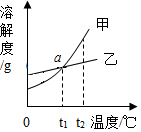
(3)如图是甲、乙两种固体物质(甲、乙均不含结晶水)在水中的溶解度曲线图.
①a点表示的意义是t1℃时甲、乙两物质的溶解度相等.
②将t1℃时甲、乙两物质的饱和溶液升温到t2℃,其溶液中溶质质量分数大小关系是甲=乙.(填“>”、“<”或“=”)
(4)化学实验中,水除了用于溶解物质外,你还知道水的用途有用作反应物(答一种即可)
分析 (1)自然界中的水中含有一些溶于水的物质;
加热煮沸时,水中的钙离子、镁离子能够以碳酸钙沉淀、氢氧化镁沉淀的形式从水中析出,从而降低水的硬度;
(2)镁离子能和氢氧根离子结合成氢氧化镁沉淀,钡离子能和硫酸根离子结合成硫酸钡沉淀,碳酸根离子能够钙离子结合成碳酸钙沉淀,能和钡离子结合成碳酸钡沉淀,氢氧化钠和稀盐酸反应生成氯化钠和水,碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳;
(3)两种物质溶解度曲线的交点表示该温度下两种物质的溶解度相等;
饱和溶液的溶质质量分数=$\frac{溶解度}{100g+溶解度}$×100%;
(4)水能和二氧化碳反应生成碳酸,电解水生成氢气和氧气.
解答 解:(1)自然界的水因为溶解了一些杂质,一般都不是纯净物;
含有较多可溶性钙、镁化合物的水叫硬水,生活中一般采用加热煮沸的方法把硬水转化为软水.
故填:纯净物;加热煮沸.
(2)上述操作按合理顺序为:加入过量NaOH溶液除去镁离子,加入过量BaCl2溶液除去硫酸根离子,加入过量Na2CO3溶液除去钙离子和过量的钡离子,过滤除去氢氧化镁、碳酸钙、硫酸钡和碳酸钡,加入适量稀盐酸除去过量的氢氧化钠和碳酸钠.
故填:④③⑤①.
(3)①a点表示的意义是t1℃时甲、乙两物质的溶解度相等.
故填:t1℃时甲、乙两物质的溶解度相等.
②t1℃时甲、乙两物质的溶解度相等,因此甲、乙两物质的饱和溶液的溶质质量分数相等,t1℃时甲、乙两物质的饱和溶液升温到t2℃时,由于都变成不饱和溶液,质量分数都不变,因此其溶液中溶质质量分数大小关系是甲=乙.
故填:=.
(4)化学实验中,水除了用于溶解物质外,还可以用作反应物.
故填:用作反应物.
点评 (2)中,②④的顺序可以颠倒,而④③的顺序不能颠倒,这是因为如果④③顺序颠倒,则过量的氯化钡不能除去,要注意理解.

| A. | 木材能燃烧 | B. | 水的沸点通常是100℃ | ||
| C. | 矿石粉碎 | D. | 二氧化碳使澄清的石灰水变浑浊 |
| A. | 汞 | B. | 氢气 | C. | 水 | D. | 二氧化碳 |
| A. | 煮沸 | B. | 过滤 | C. | 吸附 | D. | 沉淀 |
| A. | H | B. | H2 | C. | Fe | D. | 、Cl |
 用如图装置完成以下实验:
用如图装置完成以下实验:
 是元素的原子结构示意图,其相对原子质量为32.06,该原子在化学反应中易得到(填“得到”或“失去”)电子.
是元素的原子结构示意图,其相对原子质量为32.06,该原子在化学反应中易得到(填“得到”或“失去”)电子.
