题目内容
9.元素周期表是学习和研究化学的重要工具.下表是元素周期表中的一部分,请按表中信息填空:
(1)原子序数是元素周期表按元素原子核电荷数递增的顺序给元素编的号.原子序数与元素原子核电荷数在数值上相同.则原子序数为6的元素在上表中的位置应是①(填①、②或③),其原子核外有2个电子层.
(2)
 是元素的原子结构示意图,其相对原子质量为32.06,该原子在化学反应中易得到(填“得到”或“失去”)电子.
是元素的原子结构示意图,其相对原子质量为32.06,该原子在化学反应中易得到(填“得到”或“失去”)电子.(3)表中不同种元素最本质的区别是A(填字母).
A.质子数不同 B.相对原子质量不同 C.中子数不同
(4)表中第三周期的原子结构中最外层电子数的变化规律从左到右最外层电子数依次增加.
(5)已知元素周期表中,同一纵行中元素化学性质相似,其原因是同一纵行的中元素的最外层电子数相等,则氟元素最外层有7个电子.
分析 (1)根据题意,原子序数是元素周期表按元素原子核电荷数递增的顺序给元素编的号,原子序数与元素原子核电荷数在数值上相同,据此进行分析解答.
(2)由原子结构示意图为可以看出:圆圈内的数字是16,该元素原子核内有16个质子,结合若原子的最外层电子数≥4,在化学反应中易得电子,若最外层电子数<4,在化学反应中易失去电子,进行分析解答.
(3)根据元素的含义进行解答.
(4)根据表中各元素最外层电子数的特点分析规律.
(5)根据题干信息来分析解答.
解答 解:(1)原子序数是元素周期表按元素原子核电荷数递增的顺序给元素编的号,原子序数与元素原子核电荷数在数值上相同,则原子序数为6的元素在上表中的位置应是①.位于第二周期,则原子核外有2个电子层;故填:①;2;
(2)由元素周期表的信息可知,硫的相对原子质量为32.06,由原子结构示意图为可以看出:圆圈内的数字是16,该元素原子核内有16个质子;由原子序数=核电荷数=质子数,则该元素的原子序数为16,为硫元素.最外层电子数是6,在化学反应中易得到2个电子而形成阴离子.故填:32.06;得到;
(3)元素是指具有相同质子数或核电荷数的同一类原子的总称,所以表中不同种元素最本质的区别是质子数不同,故选A.
(4)观察表中第三周期各元素最外层电子数的变化可以看出最外层电子数从左到右由1递增到8.故填:从左到右最外层电子数依次增加;
(5)氟原子的最外层有7个电子,故填:7.
点评 本题考查学生根据原子结构示意图分析总结元素周期律及对元素的性质与最外层电子数的关系的理解与掌握,并能在解题中灵活应用.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
14.化学小组同学在加热二氧化锰样品时,发现有气泡产生(如图一所示),于是他们对这个异常现象进行了探究.

(1)对气体成分的探究:加热二氧化锰样品,将产生的气体通入澄清的石灰水,发现石灰水变浑浊,反应的化学方程式是CO2+Ca(OH)2═CaCO3↓+H2O,由此可知:产生的气体是二氧化碳.
(2)对气体来源的探究:
【假设1】甲同学认为:该气体来自于试管中的空气,请你设计实验证明该假设不成立
【假设2】乙同学认为产生气体的原因是二氧化锰中含有杂质.根据药品的颜色猜想,二氧化锰样品中可能混有炭粉(填物质名称)发生反应生成了该气体.他设计了如图二所示的实验进行研究,其中B装置的作用是检验A中反应是否完全,B中的试剂是澄清石灰水,A中发生化学反应的化学方程式是CO2+2NaOH═Na2CO3+H2O 实验中观察到D处澄清石灰水变浑浊.他又用氮气代替空气(氮气不参与该实验中的任何反应),重复上述实验,发现D处澄清的石灰水不变浑浊.
【结论】通过乙同学的实验证明,乙同学的猜想是正确的,二氧化锰中含有的杂质可能与炭粉或二氧化锰反应产生了这种气体.

(1)对气体成分的探究:加热二氧化锰样品,将产生的气体通入澄清的石灰水,发现石灰水变浑浊,反应的化学方程式是CO2+Ca(OH)2═CaCO3↓+H2O,由此可知:产生的气体是二氧化碳.
(2)对气体来源的探究:
【假设1】甲同学认为:该气体来自于试管中的空气,请你设计实验证明该假设不成立
| 实验步骤及现象 | 结论 |
| 假设不成立. |
【结论】通过乙同学的实验证明,乙同学的猜想是正确的,二氧化锰中含有的杂质可能与炭粉或二氧化锰反应产生了这种气体.
1.下列图象能正确反映其相应变化过程的是( )
| A. |  表示实验室用KClO3与MnO2共热制O2 表示实验室用KClO3与MnO2共热制O2 | |
| B. |  表示将水通电电解一段时间 表示将水通电电解一段时间 | |
| C. |  表示向一定量的氢氧化钠和氯化钡的混合溶液中滴加稀硫酸 表示向一定量的氢氧化钠和氯化钡的混合溶液中滴加稀硫酸 | |
| D. |  表示一定质量的稀硫酸中不断加入氧化铜固体 表示一定质量的稀硫酸中不断加入氧化铜固体 |
19.下列实验现象描述正确的是( )
| A. | 铁丝插入硫酸铜溶液,铁丝表面覆盖一层红色物质,溶液由浅绿色变成蓝色 | |
| B. | 电解水时正极产生的气体比负极产生的气体少 | |
| C. | 一氧化碳通入灼热氧化铜,黑色粉末变红色,且产生二氧化碳 | |
| D. | 硫在空气中燃烧,产生明亮的蓝紫色火焰,生成一种有刺激性气味的气体 |
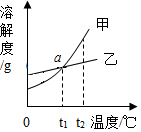
 如图是A、B两种固体物质的溶解度曲线.据图回答:
如图是A、B两种固体物质的溶解度曲线.据图回答:

 水是生命之源,也是一种重要的资源,日常生活、工农业生产和科学实验都离不开水,请回答下列问题:
水是生命之源,也是一种重要的资源,日常生活、工农业生产和科学实验都离不开水,请回答下列问题: