题目内容
11.若有溶质质量分数为20%的氯化钠溶液100kg(密度是ag/cm3),要将其变成以满足生产需要的10%的氯化钠溶液,请写出主要操作步骤(不需要具体数值).分析 溶液稀释前后,溶质质量不变.
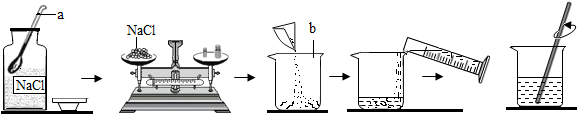
解答 解:若有溶质质量分数为20%的氯化钠溶液100kg(密度是ag/cm3),要将其变成以满足生产需要的10%的氯化钠溶液,主要操作步骤是:计算:需要氯化钠质量为:100kg×20%=20kg,需要水的体积为:(20kg÷10%-20kg)÷1kg/L=180L,称量:称量20kg氯化钠,量取180L水,溶解:把氯化钠和水放入容器中,利用玻璃棒搅拌使氯化钠完全溶解.
故答案为:计算、称量、溶解.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
5.为了测定某碳酸钠样品(其中杂质为氯化钠)的质量分数,小明同学进行了三次实验,反应的化学方程方程式为:Na2CO3+CaCl2=CaCO3↓+2NaCl.实验数据如下表:
根据上表内数据,完成下列有关计算:
(1)碳酸钠样品中碳酸钠的质量是4.24g.
(2)碳酸钠样品中杂质氯化钠的质量分数是15.2%.
(3)加入氯化钙溶液的溶质质量分数是多少?(请根据化学方程式写出完整的计算步骤)
| 编 号 | 第1次 | 第2次 | 第3次 |
| 所取固体样品的质量/g | 7 | 5 | 5 |
| 加入氯化钙溶液的质量/g | 50 | 50 | 75 |
| 反应后生成沉淀的质量/g | 4 | 4 | 4 |
(1)碳酸钠样品中碳酸钠的质量是4.24g.
(2)碳酸钠样品中杂质氯化钠的质量分数是15.2%.
(3)加入氯化钙溶液的溶质质量分数是多少?(请根据化学方程式写出完整的计算步骤)
16.20℃时,在盛有50g水的烧杯中加入15g固体X(不含杂质),充分溶解后,逐渐升温,并测定不同温度时析出固体X的质量.测定结果记录如表:
若不考虑水蒸发对实验的影响,请回答下列问题.
(1)35℃时,该溶液的质量是57g;
(2)65℃时,该溶液是Ⅲ(选填编号);
Ⅰ.饱和溶液Ⅱ.不饱和溶液Ⅲ.无法判断
(3)根据下表溶解度与溶解性的关系,可知X属于可溶物质;
(4)50℃时,使烧杯中析出的5g固体X全部溶解,至少加入25g水.
| 溶液的温度/℃ | 20 | 35 | 50 | 65 | 75 |
| 析出固体X的质量/g | 10.4 | 8.0 | 5.0 | 0 | 0 |
(1)35℃时,该溶液的质量是57g;
(2)65℃时,该溶液是Ⅲ(选填编号);
Ⅰ.饱和溶液Ⅱ.不饱和溶液Ⅲ.无法判断
(3)根据下表溶解度与溶解性的关系,可知X属于可溶物质;
| 溶解性 | 易溶 | 可溶 | 微溶 | 难溶(或不溶) |
| 溶解度(20℃) | >10 | 1-10 | 0.01-1 | <0.01 |
3.下列说法中正确的是( )
| A. | 饱和溶液降温析出晶体后,溶质质量分数一定减小 | |
| B. | t℃某饱和的氢氧化钙溶液加入少量的生石灰,充分反应后,恢复到t℃,则溶液的质量不变 | |
| C. | 将密度为1.84 g/cm3溶质质量分数为98%的浓硫酸稀释为49%的硫酸,所加水的体积与所取浓硫酸的体积一定相等 | |
| D. | MgO与CuO的混合物与98g10%的稀硫酸恰好完全反应,则原混合物中氧元素的质量是1.6g |
20.某化学兴趣小组通过实验测出:正常环境下,人所吸入空气中各种气体的体积分数如表所示:则表格中Y气体最有可能是( )
| 气体 | 吸入气体 |
| X | 78% |
| Y | 21% |
| Z | 0.03% |
| W | 0.06% |
| 其他 | 0.91% |
| A. | 氧气 | B. | 稀有气体 | C. | 氮气 | D. | 二氧化碳 |