题目内容
7. 铜、铁、铝是生产生活中广泛使用的金属.
铜、铁、铝是生产生活中广泛使用的金属.(1)每年因金属锈蚀造成很大浪费,钢铁生锈实际是铁与空气中的氧气和水蒸气发生化学反应,所以常在钢铁表面采取镀上一层不易锈蚀的金属措施(只写一种),以防止钢铁生锈.
(2)如图是铝元素在元素周期表中的相关信息及其原子的结构示意图:
①如果把铝的相对原子质量近似为27,则氯原子的中子数为14;氯原子在化学反应中容易失电子成为铝离子(填“得”或“失”,铝离子符号为Al3+.
②在空气中打磨过的铝丝表面逐渐变暗,此变化过程可用化学方程式表示为4Al+3O2═2Al2O3.
(3)年代久远的铜器表面往往生有绿色铜锈,其主要成分是碱式碳酸铜[Cu2(OH)2CO3],化学性质类似于碱和碳酸盐.可用稀盐酸除去铜器表面上的铜锈,反应生成蓝色溶液和无色气体.写出稀硫酸和碱式碳酸铜反应的化学方程式:Cu2(OH)2C03+2H2S04=2CuS04+CO2↑+3H2O.
分析 (1)钢铁生锈实际是铁与空气中的氧气和水分发生化学反应的结果;
(2)根据元素周期表和原子结构来分析,结合化学方程式书写方法来分析;
(3)依据碱式碳酸铜具备碱和碳酸盐的性质分析该物质与酸反应的产物.
解答 解:(1)钢铁生锈实际是铁与空气中的氧气和水蒸气发生了化学反应,所以在钢铁表面镀上一层不易锈蚀的金属等能防止钢铁生锈.故填:氧气和水蒸气;镀上一层不易锈蚀的金属;
(2)①相对原子质量=质子数+中子数,中子数=27-13=14;其原子结构中最外层有3个电子,在化学反应中易失去3个电子形成带三个单位正电荷的铝离子;
故填:14;失;Al3+;
②打磨过的光亮铝条置于空气中,表面逐渐变暗,铝与氧气发生氧化反应:4Al+3O2═2Al2O3;故填:4Al+3O2═2Al2O3;
(3)由于碱式碳酸铜具备碱和碳酸盐的性质,所以[Cu2(OH)2CO3]和硫酸反应的产物是硫酸铜、水和二氧化碳,方程式为Cu2(OH)2C03+2H2S04=2CuS04+CO2↑+3H2O;故填:Cu2(OH)2C03+2H2S04=2CuS04+CO2↑+3H2O.
点评 本题难度不大,考查学生根据反应原理书写化学方程式的能力,掌握化学方程式的书写方法即可正确解答本题.

练习册系列答案
相关题目
8.下列说法正确的是( )
| A. | 使用金属来制作炊具,是利用了其化学性质 | |
| B. | 自然界的水都或多或少含有杂质,所以最健康的饮用水就是蒸馏水 | |
| C. | 空气中含有的元素质量分数最大的是氧 | |
| D. | 地表上能够以游离态存在的金属元素只能是很不活泼的少数几种 |
15.世界卫生组织将5月31日定为“世界无烟日”,吸烟有害健康.我国遭受二手烟危害的非吸烟人口就多达7.4亿.烟雾中主要含有一氧化碳、尼古丁(C10H14N2)和焦油,这三种物质倍称为香烟的三大杀手.下列有关说法中,正确的是( )
①生活中应拒绝毒品 ②焦油能诱发细胞病变 ③吸烟对他人无害
④“煤气”中毒是由一氧化碳引起的 ⑤在尼古丁中氮元素的含量最高.
①生活中应拒绝毒品 ②焦油能诱发细胞病变 ③吸烟对他人无害
④“煤气”中毒是由一氧化碳引起的 ⑤在尼古丁中氮元素的含量最高.
| A. | ①②④ | B. | ①②③ | C. | ①④⑤ | D. | ②③⑤ |
2.某化学课堂围绕“酸碱中和反应”,将学生分成若干小组,在老师引导下开展探究活动.以下是教学片断.请你参与学习并帮助填写空格.
【演示实验】将一定量的稀H2SO4加入到盛有NaOH溶液的小烧杯中.
【学生板演】该反应的化学方程式:H2SO4+2NaOH═Na2SO4+2H2O.
【提出问题】实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质是什么呢?
【假设猜想】针对疑问,大家纷纷提出猜想.甲组同学的猜想如下,请你补上猜想四.
猜想一:只有Na2SO4 猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4、H2SO4和NaOH 猜想四:有Na2SO4和NaOH
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的.不合理的猜想是三,理由是稀硫酸和氢氧化钠不能共存.
【实验探究】
(1)丙组同学取烧杯中的溶液少量于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有氢氧化钠.
(2)为了验证其余猜想,各学习小组利用烧杯中的溶液,并选用老师提供的pH试纸、铜片、AgNO3溶液、Na2CO3溶液,进行如下三个方案的探究.
【得出结论】通过探究,全班同学一致确定猜想二是正确的.
【评价反思】老师对同学们能用多种方法进行探究,并且得出正确结论给予肯定.同时指出(2)中存在两处明显错误,请大家反思.同学们经过反思发现了这两处错误:
(1)实验操作中的错误是把pH试纸浸入溶液中.
(2)实验方案中也有一个错误的,错误的原因是硫酸钠也能够和氯化钡反应生成硫酸钡沉淀.
【演示实验】将一定量的稀H2SO4加入到盛有NaOH溶液的小烧杯中.
【学生板演】该反应的化学方程式:H2SO4+2NaOH═Na2SO4+2H2O.
【提出问题】实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质是什么呢?
【假设猜想】针对疑问,大家纷纷提出猜想.甲组同学的猜想如下,请你补上猜想四.
猜想一:只有Na2SO4 猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4、H2SO4和NaOH 猜想四:有Na2SO4和NaOH
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的.不合理的猜想是三,理由是稀硫酸和氢氧化钠不能共存.
【实验探究】
(1)丙组同学取烧杯中的溶液少量于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有氢氧化钠.
(2)为了验证其余猜想,各学习小组利用烧杯中的溶液,并选用老师提供的pH试纸、铜片、AgNO3溶液、Na2CO3溶液,进行如下三个方案的探究.
| 实验方案 | 测溶液的pH | 滴加Na2CO3溶液 | 滴加BaCl2溶液 |
| 实验操作 |  | 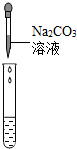 | 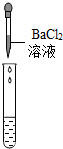 |
| 实验现象 | 试纸变色,对比比色卡,pH=1 | 有气泡产生 | 产生白色沉淀 |
| 实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中有H2SO4 |
【评价反思】老师对同学们能用多种方法进行探究,并且得出正确结论给予肯定.同时指出(2)中存在两处明显错误,请大家反思.同学们经过反思发现了这两处错误:
(1)实验操作中的错误是把pH试纸浸入溶液中.
(2)实验方案中也有一个错误的,错误的原因是硫酸钠也能够和氯化钡反应生成硫酸钡沉淀.
19.下列变化中属于化学变化的是( )
| A. |  榨取果汁 | B. |  粉碎废纸 | C. |  沙里淘金 | D. |  燃放烟花 |
16. 有关物质之间的部分转化关系如图所示.其中“-”表示物质之间能发生化学反应,“→”表示物质之间的转化关系.下列说法中正确的是( )
有关物质之间的部分转化关系如图所示.其中“-”表示物质之间能发生化学反应,“→”表示物质之间的转化关系.下列说法中正确的是( )
 有关物质之间的部分转化关系如图所示.其中“-”表示物质之间能发生化学反应,“→”表示物质之间的转化关系.下列说法中正确的是( )
有关物质之间的部分转化关系如图所示.其中“-”表示物质之间能发生化学反应,“→”表示物质之间的转化关系.下列说法中正确的是( )| A. | 物质X是一种常见的有机化合物 | |
| B. | 图中的所有反应均不属于置换反应 | |
| C. | 向Ca(OH)2溶液中加入CaO,所得溶液的溶质质量分数一定增大 | |
| D. | 反应②是一定有盐参加反应 |
 如图表示的是物质A-H相互间的关系(“→”表示物质间的转化关系,“-”表示两端的物质能发生化学反应).A、G都是单质,气体C常用于灭火,F是一种蓝色溶液常和E一起用于配制农药波尔多液.请你回答:
如图表示的是物质A-H相互间的关系(“→”表示物质间的转化关系,“-”表示两端的物质能发生化学反应).A、G都是单质,气体C常用于灭火,F是一种蓝色溶液常和E一起用于配制农药波尔多液.请你回答: