题目内容
2.如图1是金属活动性顺序表中铜、锡、铁和铝元素被人类大规模开发、利用的大致年限.(1)选择编号填空:铝的利用比铜和铁 晚得多,原因是②;铝在多个 领域替代易生锈的钢铁,其主要原因是④.
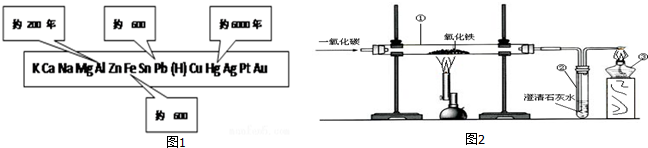
①铝的硬度小②铝很活泼③地壳中铝的含量高④铝的表面易生成致密的保护膜
(2)钢铁的冶炼是人类文明的一个重要标志.如图2是实验室模拟炼铁的装置图,试回答下列问题:
实验中看到的实验现象为:玻璃管中的粉末红色粉末变黑试管里的澄淸石灰水变浑浊.
(3)玻璃管中反应的化学方程式为3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$3CO2+2Fe.
(4)加热氧化铁之前,先通一会儿一氧化碳的作用是排出空气,防止加热时爆炸.
(5)该实验设计装置③的目的是除去尾气中的CO,防止污染空气.
分析 (1)金属越活泼,越不易冶炼出来,铝虽然活动性比铁强,但是表面有致密的氧化物薄膜而导致不易生锈.
(2)根据实验室模拟炼铁的装置图,写出冶炼生铁的化学方程式,根据炼铁时的注意事项分析解答;如果通入一氧化碳过量,存在有毒尾气未处理的缺陷.
解答 解:
(1)在金属活动性顺序中,铝>铁>铜,金属越活泼,越不易冶炼出来,故铝的利用比铜和铁晚得多,铝虽然活动性比铁强,但是表面有致密的氧化物薄膜而导致不易生锈;
(2)氧化铁在一氧化碳的还原作用下,红色氧化铁粉末变成黑色铁粉末;二氧化碳能使澄清的石灰水变浑浊;
(3)由图可知,此反应为一氧化碳还原氧化铁,反应的方程式是:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$3CO2+2Fe;
(4)加热氧化铁之前,先通一会儿一氧化碳的作用是排出空气,防止加热时爆炸;
(5)一氧化碳有毒,易燃,可用点燃的方法去除尾气.该实验设计装置③的目的是除去尾气中的CO,防止污染空气.
答案:
(1)②; ④;
(2)红色粉末变黑; 变浑浊;
(3)Fe2O3+3CO═2Fe+3CO2
(4)排出空气,防止加热时爆炸;
(5)除去尾气中的CO,防止污染空气.
点评 本题考查了高炉炼铁的原理以及实验中的注意点,更高层次的要求设计实验(证明铁产生)以及实际搭建装置的实验操作能力.

练习册系列答案
相关题目
13.下列概念中,前者一定包括后者的是( )
| A. | 化合反应 氧化反应 | B. | 氧化反应 缓慢氧化 | ||
| C. | 混合物 纯净物 | D. | 物理性质 化学性质 |
10.为测定13.5g铝片的纯度,进行了以下实验:
取240g稀硫酸平均分成6等分,把该铝片依次投入到各分稀硫酸中,实验结果如表所示:
请计算:(1)m的数值是1.2;
(2)铝片中铝的质量分数.
取240g稀硫酸平均分成6等分,把该铝片依次投入到各分稀硫酸中,实验结果如表所示:
| 次数 | 1 | 2 | 3 | 4 | 5 | 6 |
| 稀硫酸的质量(g) | 40 | 40 | 40 | 40 | 40 | 40 |
| 生成H2的质量(g) | 0.3 | 0.6 | 0.9 | 1.2 | m | 1.2 |
(2)铝片中铝的质量分数.
11.以下说法正确的是( )
| A. | 常温下金属都是固体 | |
| B. | 铝比铁抗腐蚀能力强,铝没有铁活泼 | |
| C. | 青铜、生铁、焊锡均属合金 | |
| D. | 木炭和ZnO在高温条件下不能反应 |
12.如图实验操作正确的是( )
| A. |  滴加液体 | B. |  量取液体体积读数 | ||
| C. |  二氧化碳验满 | D. |  测定溶液的pH |
 生活中处处充满了化学.如图所示是医院常用的药瓶和注射器,请你据图中名称回答:
生活中处处充满了化学.如图所示是医院常用的药瓶和注射器,请你据图中名称回答: