题目内容
7.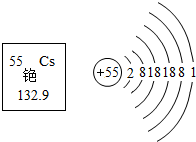 铯原子钟2000万年仅误差1秒,它的工作原理是利用铯原子内部的电子在两个能级间跳跃时辐射出的电磁波来控制钟的走动.如图所示为铯元素的相关信息.下列说法正确的是( )
铯原子钟2000万年仅误差1秒,它的工作原理是利用铯原子内部的电子在两个能级间跳跃时辐射出的电磁波来控制钟的走动.如图所示为铯元素的相关信息.下列说法正确的是( )| A. | 原子核内中子数为133 | B. | 该元素的原子序数为55 | ||
| C. | 铯离子Cs+核外有55个电子 | D. | 铯属于非金属元素,位于第六周期 |
分析 原子结构示意图中,圆圈内数字表示核内质子数,弧线表示电子层,弧线上的数字表示该层上的电子数,离圆圈最远的弧线表示最外层.若最外层电子数≥4,在化学反应中易得电子,若最外层电子数<4,在化学反应中易失去电子.根据元素周期表中的一个小格信息可知元素的名称、元素符号、原子序数、相对原子质量,然后利用原子序数等于质子数等来分析解答即可.
解答 解:A.由元素周期表和原子结构示意图无法确定某原子核内的中子数,133是该元素原子的近似相对原子质量,故错误;
B.由元素周期表的信息可知,该元素的原子序数为55,故正确;
C.铯原子核外有55个电子,最外层有1个电子,在化学反应中易失去一个电子,而形成带一个单位正电荷的阳离子,此时离子核外有54个电子,故错误;
D.由元素的名称“铯”字偏旁可知,该元素属于金属元素,故错误.
故选B.
点评 本题难度不大,考查学生对元素周期表、原子结构示意图及其意义的理解,了解元素周期表和原子结构示意图的意义是正确解题的关键.

练习册系列答案
 计算高手系列答案
计算高手系列答案
相关题目
17.下列物质难溶于水的是( )
| A. | K2SiO3 | B. | Hg(NO3)2 | C. | (NH4)2S | D. | Mn(OH)2 |
16.氢氧化铯是一种可溶性碱,其化学式为CsOH,则有关的下列叙述中,错误的是( )
| A. | CsOH在水溶液中的电离方程式为:CsOH═Cs++OH- | |
| B. | CsOH溶液能使酚酞试液变红 | |
| C. | 因为CsCl是易溶于水的盐,所以CsOH溶液与稀盐酸不发生复分解反应 | |
| D. | CsOH溶液与MgCl2溶液发生复分解反应,有氢氧化镁沉淀生成 |