题目内容
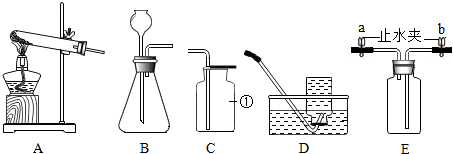
19.实验室开放日,某化学兴趣小组的同学在老师的指导下,设计了如下实验装置进行气体制取和性质的探究,请回答有关问题: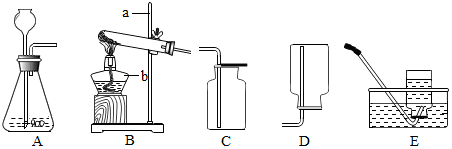
(1)请写出图中标有字母的仪器名称:
a铁架台; b酒精灯.
(2)实验室用氯酸钾和二氧化锰混合物加热制取氧气时,应选用的发生装置是B(填写装置的字母代号,下同),其中二氧化锰起催化作用.请写出该反应的文字表达式:氯酸钾$\stackrel{二氧化锰}{→}$氯化钾+氧气.
(3)如果用装置E收集气体结束后应先撤导管再熄灭酒精灯.
(4)若实验室用高锰酸钾为原料制取氧气选用的装置是B,指出装置中的一个不足是导管口没有放一小团棉花,这样会导致的后果是高锰酸钾颗粒进入导管.
分析 (1)根据常见仪器的名称和用途进行解答;
(2)根据实验室用氯酸钾与二氧化锰的混合物制取氧气需要加热及二氧化锰的作用,文字表达式的书写等进行解答;
(3)根据装置E收集气体时的注意事项进行解答;
(4)根据用加热高锰酸钾的方法制取氧气时的注意事项进行解答.
解答 解:(1)图中标有字母的仪器名称:a是铁架台;b是酒精灯;故填:a铁架台;b酒精灯;
(2)实验室用氯酸钾与二氧化锰的混合物制取氧气需要加热,所以发生装置选择B;二氧化锰的作用是催化作用,该反应的文字表达式:氯酸钾$\stackrel{二氧化锰}{→}$氯化钾+氧气;故填:B;催化;氯酸钾$\stackrel{二氧化锰}{→}$氯化钾+氧气;
(3)用装置E收集气体结束后应先撤导管,后熄灭酒精灯,防止水被倒吸入反应装置造成装置炸裂;故填:撤导管;熄灭酒精灯;
(4)用高锰酸钾为原料制取氧气要加热,故选用的装置是B,装置中的一个不足是导管口没有放一小团棉花,这样会导致的后果是高锰酸钾颗粒会进入导管之中,故填:B;导管口没有放一小团棉花;高锰酸钾颗粒进入导管;
点评 反应装置的选择主要依据反应物的状态以及反应是否需要加热,收集装置的选择主要依据气体的密度以及是否能溶于水,并掌握实验室制取氧气、二氧化碳的反应原理、注意事项.

练习册系列答案
 华东师大版一课一练系列答案
华东师大版一课一练系列答案
相关题目
7.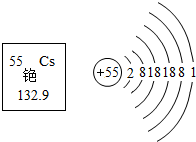 铯原子钟2000万年仅误差1秒,它的工作原理是利用铯原子内部的电子在两个能级间跳跃时辐射出的电磁波来控制钟的走动.如图所示为铯元素的相关信息.下列说法正确的是( )
铯原子钟2000万年仅误差1秒,它的工作原理是利用铯原子内部的电子在两个能级间跳跃时辐射出的电磁波来控制钟的走动.如图所示为铯元素的相关信息.下列说法正确的是( )
 铯原子钟2000万年仅误差1秒,它的工作原理是利用铯原子内部的电子在两个能级间跳跃时辐射出的电磁波来控制钟的走动.如图所示为铯元素的相关信息.下列说法正确的是( )
铯原子钟2000万年仅误差1秒,它的工作原理是利用铯原子内部的电子在两个能级间跳跃时辐射出的电磁波来控制钟的走动.如图所示为铯元素的相关信息.下列说法正确的是( )| A. | 原子核内中子数为133 | B. | 该元素的原子序数为55 | ||
| C. | 铯离子Cs+核外有55个电子 | D. | 铯属于非金属元素,位于第六周期 |
14.如图:这四位同学描述的是同一化学符号,此化学符号是( )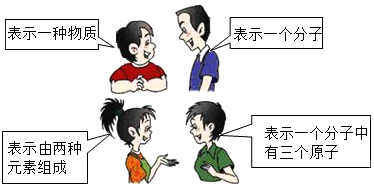

| A. | O3 | B. | HClO | C. | NO | D. | H2O |
8. 红枣包装中常使用一种袋装防腐剂,品名为“504双吸剂”,其标签如图所示.同学们对一包久置的“504双吸剂”固体样品很好奇,设计实验进行探究.
红枣包装中常使用一种袋装防腐剂,品名为“504双吸剂”,其标签如图所示.同学们对一包久置的“504双吸剂”固体样品很好奇,设计实验进行探究.
【提出问题】久置固体的成分是什么?
【查阅资料】铁与氯化铁溶液在常温下发生反应生成氯化亚铁.
【猜想】久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3.
【实验探究1】甲同学的方案:
【实验质疑】
(1)乙同学认为甲同学的实验中不能得出一定含Ca(OH)2的结论,理由是氧化钙与水反应生成的氢氧化钙也能使无色酚酞变红,不能确定原固体中是否含有氢氧化钙.
(2)丙同学认为甲同学的实验并不能得出一定不含Fe2O3的结论,理由是氧化铁和盐酸反应生成氯化铁,铁和氯化铁反应生成氯化亚铁,溶液也是浅绿色.
【实验探究2】
乙、丙同学设计如下实验方案继续验证:

(1)③中反应的化学方程式是Na2CO3+Ca(OH)2=CaCO3↓+2NaOH.
(2)乙、丙同学实验中能得出固体样品中一定还含有,仍有一种物质不能确定,该物质是Ca(OH)2.
(3)乙、丙同学又经过实验测得上述残留固体中含钙物质的总质量为1.6g,滤渣B中CaCO3的质量为1.0g,滤渣C的质量为1.0g.
【实验结论】综合上述实验及所给数据,久置固体的成分是Fe、Fe2O3、CaO、Ca(OH)2、CaCO3.
 红枣包装中常使用一种袋装防腐剂,品名为“504双吸剂”,其标签如图所示.同学们对一包久置的“504双吸剂”固体样品很好奇,设计实验进行探究.
红枣包装中常使用一种袋装防腐剂,品名为“504双吸剂”,其标签如图所示.同学们对一包久置的“504双吸剂”固体样品很好奇,设计实验进行探究.【提出问题】久置固体的成分是什么?
【查阅资料】铁与氯化铁溶液在常温下发生反应生成氯化亚铁.
【猜想】久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3.
【实验探究1】甲同学的方案:
| 实验操作 | 实验现象 | 实验结论 |
| (1)取少量固体放于试管中,加足量蒸馏水溶解,静置后取上层清液滴加无色酚酞溶液 | 固体溶解时试管外壁发烫,试管底部有不溶物,溶液变红 | 固体中一定含有 和Ca(OH)2. |
| (2)另取少量固体放于试管中,滴加足量的 | 固体逐渐消失,有无色气体产生,得到浅绿色溶液 | 固体中一定含有Fe,一定不含Fe2O3 |
| (3)将步骤(2)中产生的气体通入到澄清石灰水中 | 固体中一定含有CaCO3 |
(1)乙同学认为甲同学的实验中不能得出一定含Ca(OH)2的结论,理由是氧化钙与水反应生成的氢氧化钙也能使无色酚酞变红,不能确定原固体中是否含有氢氧化钙.
(2)丙同学认为甲同学的实验并不能得出一定不含Fe2O3的结论,理由是氧化铁和盐酸反应生成氯化铁,铁和氯化铁反应生成氯化亚铁,溶液也是浅绿色.
【实验探究2】
乙、丙同学设计如下实验方案继续验证:

(1)③中反应的化学方程式是Na2CO3+Ca(OH)2=CaCO3↓+2NaOH.
(2)乙、丙同学实验中能得出固体样品中一定还含有,仍有一种物质不能确定,该物质是Ca(OH)2.
(3)乙、丙同学又经过实验测得上述残留固体中含钙物质的总质量为1.6g,滤渣B中CaCO3的质量为1.0g,滤渣C的质量为1.0g.
【实验结论】综合上述实验及所给数据,久置固体的成分是Fe、Fe2O3、CaO、Ca(OH)2、CaCO3.
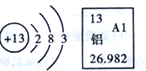 如图表示同一种元素Al,据图回答:
如图表示同一种元素Al,据图回答: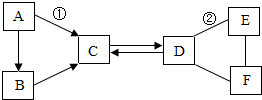 A~F是初中化学中常见的六种物质,其中B、C组成元素相同,C、D、E、F是不同类别的化合物,D和E的溶液均呈碱性,且E可用作建筑材料,它们相互间的关系如图所示,(图中“-”表示相连的物质两两之间可以发生反应,“→”表示由某一物质转化为另一物质,部分反应物、生成物及反应条件已略去).
A~F是初中化学中常见的六种物质,其中B、C组成元素相同,C、D、E、F是不同类别的化合物,D和E的溶液均呈碱性,且E可用作建筑材料,它们相互间的关系如图所示,(图中“-”表示相连的物质两两之间可以发生反应,“→”表示由某一物质转化为另一物质,部分反应物、生成物及反应条件已略去). 今年我国纪念“世界水日”和“中国水周”活动的宣传主题为“节约水资源,保障水安全”.
今年我国纪念“世界水日”和“中国水周”活动的宣传主题为“节约水资源,保障水安全”.