题目内容
2.下列关于“酒精温度计遇冷读数下降”的微观解释正确的是( )| A. | 分子停止运动 | B. | 分子体积缩小 | ||
| C. | 分子种类发生变化 | D. | 分子间间隙减小 |
分析 根据分子的基本特征:分子质量和体积都很小;分子之间有间隔;分子是在不断运动的;同种的分子性质相同,不同种的分子性质不同,可以简记为:“两小运间,同同不不”,结合事实进行分析判断即可.
解答 解:A、酒精温度计遇冷读数下降,是因为温度降低,酒精分子间的间隔变小,而不是分子停止运动,故选项解释错误.
B、酒精温度计遇冷读数下降,是因为温度降低,酒精分子间的间隔变小,而不是分子体积缩小,故选项解释错误.
C、酒精温度计遇冷读数下降,是因为温度降低,酒精分子间的间隔变小,而不是分子种类发生变化,故选项解释错误.
D、酒精温度计遇冷读数下降,是因为温度降低,酒精分子间的间隔变小,故选项解释正确.
故选:D.
点评 本题难度不大,掌握分子的基本性质(可以简记为:“两小运间,同同不不”)及利用分子的基本性质分析和解决问题的方法是解答此类题的关键.

练习册系列答案
 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案
相关题目
10.下列说法正确的是( )
| A. | 煤、石油、天然气是当今最重要的三大矿物燃料,是取之不尽的 | |
| B. | 煤是一种复杂的混合物,主要含有碳、氢两种元素 | |
| C. | 石油主要含有碳和氢两种元素,同时还含有少量的硫、氧、氮等元素 | |
| D. | 煤和石油都是由古代植物遗体埋在地层下或在地壳中经过一系列非常复杂的变化而形成的 |
17. 学校化学兴趣小组知道二氧化锰能做过氧化氢分解的催化剂后,想要探究两个问题:第一想探究其它一些物质如氧化铝是否也可做过氧化氢的催化剂?第二想探究不同催化剂对过氧化氢分解快慢是否有影响?请你一起参与他们的探究过程,并填写下列空白.
学校化学兴趣小组知道二氧化锰能做过氧化氢分解的催化剂后,想要探究两个问题:第一想探究其它一些物质如氧化铝是否也可做过氧化氢的催化剂?第二想探究不同催化剂对过氧化氢分解快慢是否有影响?请你一起参与他们的探究过程,并填写下列空白.
(一)(1)【问题】氧化铝能不能做过氧化氢分解的催化剂?
(2)【实验验证】
(3)【结论】氧化铝能加快过氧化氢的分解速率,故氧化铝能做过氧化氢分解的催化剂
(4)【讨论与反思】经过讨论,有的同学认为只有上述一个证据,不能证明氧化铝能作过氧化氢分解的催化剂,还要补充一个探究实验:
实验三:【实验目的】探究Al2O3在反应前后质量是否改变.
【实验步骤】①准确称量氧化铝(少量)的品质;②完成实验二③待反应结束,将实验而试管里的物质进行过滤,洗涤,干燥, ;对比反应前后氧化铝的质量.
【讨论】如果氧化铝在反应前后质量不变,则说明氧化铝可以作过氧化氢分解的催化剂.
(5)但小华认为,要证明猜想,上述三个实验还不足够,还需要再增加一个探究实验:探究Al2O3的化学性质在反应前后是否改变.
(二)(1)【问题】不同催化剂(二氧化锰和氧化铝)对过氧化氢分解快慢是否有影响?
(2)【实验验证】常温下,在同质量、同浓度的H2O2 溶液中,分别加入相同质量的MnO2和氧化铝,测量各生成一瓶(相同体积)O2 所需的时间.右下图是他们进行实验的装置图,此实验中宜采用的气体收集方法是排水法,理由是便于测定收集满一瓶气体所需时间.
(3)【实验记录】
(4)【结 论】该探究过程得出的结论是H2O2生成氧气的快慢与催化剂种类有关
(5)【讨论与反思】你认为过氧化氢分解速率的快慢还与什么因素有关?
请你举一例:过氧化氢的浓度或温度有关.
 学校化学兴趣小组知道二氧化锰能做过氧化氢分解的催化剂后,想要探究两个问题:第一想探究其它一些物质如氧化铝是否也可做过氧化氢的催化剂?第二想探究不同催化剂对过氧化氢分解快慢是否有影响?请你一起参与他们的探究过程,并填写下列空白.
学校化学兴趣小组知道二氧化锰能做过氧化氢分解的催化剂后,想要探究两个问题:第一想探究其它一些物质如氧化铝是否也可做过氧化氢的催化剂?第二想探究不同催化剂对过氧化氢分解快慢是否有影响?请你一起参与他们的探究过程,并填写下列空白.(一)(1)【问题】氧化铝能不能做过氧化氢分解的催化剂?
(2)【实验验证】
| 实验步骤 | 实验现象 | 实验结论 | |
| 实验一 | 将带火星的木条伸入装有过氧化氢溶液的试管中 | 木条不复燃 | 常温下过氧化氢溶液分解速率太慢,产生的氧气太少 |
| 实验二 | 在装有过氧化氢溶液的试管中加入少量氧化铝,再将带火星木条伸入试管中 | 木条复燃 | 加入Al2O3能加快过氧化氢溶液的分解速率 |
(4)【讨论与反思】经过讨论,有的同学认为只有上述一个证据,不能证明氧化铝能作过氧化氢分解的催化剂,还要补充一个探究实验:
实验三:【实验目的】探究Al2O3在反应前后质量是否改变.
【实验步骤】①准确称量氧化铝(少量)的品质;②完成实验二③待反应结束,将实验而试管里的物质进行过滤,洗涤,干燥, ;对比反应前后氧化铝的质量.
【讨论】如果氧化铝在反应前后质量不变,则说明氧化铝可以作过氧化氢分解的催化剂.
(5)但小华认为,要证明猜想,上述三个实验还不足够,还需要再增加一个探究实验:探究Al2O3的化学性质在反应前后是否改变.
(二)(1)【问题】不同催化剂(二氧化锰和氧化铝)对过氧化氢分解快慢是否有影响?
(2)【实验验证】常温下,在同质量、同浓度的H2O2 溶液中,分别加入相同质量的MnO2和氧化铝,测量各生成一瓶(相同体积)O2 所需的时间.右下图是他们进行实验的装置图,此实验中宜采用的气体收集方法是排水法,理由是便于测定收集满一瓶气体所需时间.
(3)【实验记录】
| 实验编号 | 1 | 2 |
| 反应物 | 5%H2O2 | 5%H2O2 |
| 催化剂 | 1g氧化铝 | 1gMnO2 |
| 时间 | 85秒 | 46秒 |
(5)【讨论与反思】你认为过氧化氢分解速率的快慢还与什么因素有关?
请你举一例:过氧化氢的浓度或温度有关.
14.咱们学校化学兴趣小组的同学,对实验室制备氧气的若干问题进行如下探究:
【探究一】为探究影响双氧水分解速率的某种因素,A小组记录了如下实验数据:
(1)写出本实验中反应的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;测量O2体积的装置是c (选填下图l中的装置编号).

(2)由实验I、II、III可知:影响双氧水分解速率的因素是:双氧水的浓度.
【探究二】B小组查阅资料:在过氧化氢溶液的分解反应中,氧化铜也能作催化剂.于是他们用天平称量0.2g氧化铜,取5%过氧化氢溶液5mL于试管中,进行如图2实验:

(1)填写如表:
(2)步骤①的目的是与步骤③对比,检验加入氧化铜前后过氧化氢溶液的分解速率有无变化,步骤④对应的实验操作是过滤,步骤⑦是证明氧化铜的化学性质在反应前后没有改变.
【探究一】为探究影响双氧水分解速率的某种因素,A小组记录了如下实验数据:
| 双氧水的质量 | 双氧水的浓度 | MnO2的质量 | 相同时间内产生O2的体积 | |
| Ⅰ | 50.0g | 1% | 0.1g | 9mL |
| Ⅱ | 50.0g | 2% | 0.1g | 16mL |
| Ⅲ | 50.0g | 4% | 0.1g | 31mL |

(2)由实验I、II、III可知:影响双氧水分解速率的因素是:双氧水的浓度.
【探究二】B小组查阅资料:在过氧化氢溶液的分解反应中,氧化铜也能作催化剂.于是他们用天平称量0.2g氧化铜,取5%过氧化氢溶液5mL于试管中,进行如图2实验:

(1)填写如表:
| 步骤③现象 | 步骤⑥结果 | 步骤⑦操作 | 结论 |
| 有大量气泡产生. | 称得氧化铜质量为0.2g. | 将固体加入盛有5mL 5%过氧化氢溶液的试管中,并把带火星的木条伸入试管,观察现象. | 在过氧化氢溶液的分解实验中,氧化铜也能作催化剂. |
11.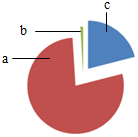 如图为空气成分示意图(按体积计算),其中“a”代表的是( )
如图为空气成分示意图(按体积计算),其中“a”代表的是( )
 如图为空气成分示意图(按体积计算),其中“a”代表的是( )
如图为空气成分示意图(按体积计算),其中“a”代表的是( )| A. | 氮气 | B. | 二氧化碳 | C. | 氧气 | D. | 稀有气体 |