��Ŀ����
5����ȡ�ס��ҡ����������ֽ�����ĩ���ֱ�Ͷ����ͬŨ�ȵ�ϡ�����У�ֻ�мס����ܲ������壬�Ҽ�����Һ���������Ƴɵ�����ʢ�ţ���ȡһС�鶡Ͷ�������������Һ�У����ı����б���������ס��ҡ����������ֽ����Ļ��˳��Ϊ��������| A�� | �ף��ң������� | B�� | �ң��ף������� | C�� | ���������ң��� | D�� | �ң��ף������� |
���� �ڽ������˳���У���ǰ�Ľ��������ᷢ���û���Ӧ����λ��Խ��ǰ����ӦԽ���ң�λ����ǰ�Ľ����ܰ�λ�����Ľ�����������Һ���û�������
��� �⣺�������֪�����ס��ҡ����������ֽ�����ĩ�ֱ�Ͷ����ͬŨ�ȵ������У�ֻ�мס��ҷ�����Ӧ���������ݣ�˵���˼ס���λ�����ǰ�ߣ�������λ����ĺ��棻�ɼ�����Һ���������Ƴɵ�����ʢ�ţ�˵�����ҵĻ�Դ��ڼף�����Ͷ�������������Һ�У����ı����б�������˵�����ڱ���ǰ�森���ԣ����ֽ����Ļ��˳��Ϊ���ң��ף�������������D��ȷ��
��ѡD��
���� ���⿼���˽������˳���Ӧ�ã���ɴ��⣬�������ݽ������˳����������У�

��ϰ��ϵ�д�
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
�����Ŀ
15����ѩ���ο�����ѩ�����������������ʳ��Ũ��ƫ�ߣ�����ܱ���ľ�����������о���һ��������ѩ���������ڻ���ѩ��������ʩ��������ľ�����ã�����²�����������õ�������ѩ���ǣ�������
| A�� | NaCl��CaCl2 | B�� | Ca��NO3��2Mg��NO3��2 | C�� | NaCl Ca��OH��2 | D�� | CaCl2MgCO3 |
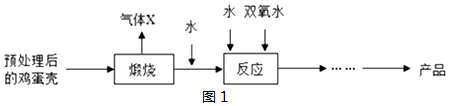
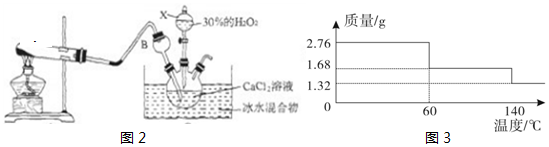
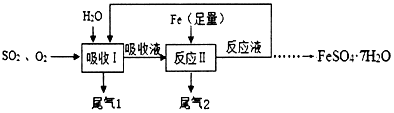
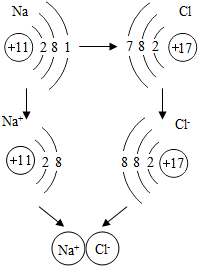 ��ͼ�ǽ�������������Ӧ�����Ȼ��Ƶ���ʾ��ͼ������ͼʾ�ش��������⣮
��ͼ�ǽ�������������Ӧ�����Ȼ��Ƶ���ʾ��ͼ������ͼʾ�ش��������⣮