题目内容
5.取等质量等质量分数的NaOH溶液和稀盐酸充分混合后,测其pH,则该液体的pH应( )| A. | 大于7 | B. | 小于7 | C. | 等于7 | D. | 无法确定 |
分析 根据化学方程式进行计算:盐酸溶液显酸性,pH小于7,氢氧化钠溶液显碱性,pH大于7.若盐酸与氢氧化钠恰好完全反应,则溶液显中性,pH=7,若酸有剩余,则溶液pH小于7,若氢氧化钠有剩余,则溶液pH大于7.
解答 解:等质量等质量分数的盐酸溶液与氢氧化钠溶液中溶质的质量相等.反应中消耗盐酸与氢氧化钠的质量比关系如下:
HCl+NaOH=NaCl+H2O
36.5 40
可以看出36.5份质量的盐酸与40份质量的氢氧化钠恰好完全反应,则等质量的盐酸与氢氧化钠混合后盐酸有剩余,溶液显酸性,pH小于7.
故选:B.
点评 酸溶液一般显酸性,碱溶液一般显碱性,但盐溶液不一定显中性,如碳酸钠属于盐,俗称纯碱,就是因为其水溶液显碱性.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
15.2012年“中国水周”的主题是:“大力加强农田水利,保障国家粮食安全”.下列认识和做法不符合这一主题的是( )
| A. | 淡水资源丰富,所以淡水可以取之不尽、用之不竭 | |
| B. | 加强工业废水的排放监控,坚持达标排放 | |
| C. | 合理施用农药、化肥,以减少水体污染 | |
| D. | 洗菜、洗衣、淘米的水用来浇花、拖地、冲厕所 |
16.在化学反应C+O2═CO2中,若生成m个CO2分子,则参加反应的氧原子的个数是( )
| A. | m | B. | 2m | C. | $\frac{m}{2}$ | D. | 4m |
20.下列表示意义和后面的化学用语一致的是( )
| A. | 两个氮原子N2 | B. | 两个氢分子2H | C. | 两个铁离子2Fe2+ | D. | 氨气NH3 |
10.下列探究的问题与设计的实验方案不相吻合的是( )
| 序号 | 探究的问题 | 实验方案 |
| A | 浓度与反应速率关系 | 分别在20%与5%的双氧水中加等量的MnO2,观察现象 |
| B | 铁金属活动性强弱 | 等质量的铁片与铁粉分别放在10%的稀盐酸中,观察现象 |
| C | 分子间隔 | 将等体积的水与酒精放在细口径的容器中,振荡,观察现象 |
| D | 物质的溶解性与溶质的性质有关 | 分别在10mL水中1~2小粒碘和高锰酸钾,振荡,观察现象 |
| A. | A | B. | B | C. | C | D. | D |
 如图装置可以用于实验室过氧化氢溶液制取氧气:此装置中长颈漏斗的作用是可随时添加过氧化氢溶液,如果用注射器代替长颈漏斗好处是可以控制反应的速度(合理即可).
如图装置可以用于实验室过氧化氢溶液制取氧气:此装置中长颈漏斗的作用是可随时添加过氧化氢溶液,如果用注射器代替长颈漏斗好处是可以控制反应的速度(合理即可).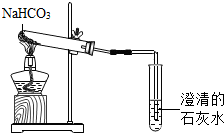 碳酸氢钠是一种重要的盐类物质,在生活中用途广泛.小红同学设计实验对碳酸氢钠的性质进行了探究.请你参与她的探究活动.
碳酸氢钠是一种重要的盐类物质,在生活中用途广泛.小红同学设计实验对碳酸氢钠的性质进行了探究.请你参与她的探究活动.