题目内容
20. 钢铁是使用最多的金属材料.
钢铁是使用最多的金属材料.(1)早在春秋战国时期,我国就开始生产和使用铁器.写出以赤铁矿(主要成分Fe2O3)为原料炼铁的化学方程式Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(2)利用新技术能将不锈钢加工成柔软的金属丝,用它和棉纤维一起编织成性能优良的劳保防护服,这是利用了不锈钢的AB(填序号).
A.耐腐蚀性B.延展性C.导热性D.导电性
(3)市场上有一种含铁粉的麦片,食用后在胃酸作用下将铁粉转化为人体可吸收的铁元素,反应的化学方程式为2HCl+Fe=H2↑+FeCl2.
(4)为探究铁和锌两种金属与酸反应的状况,将等质量的两种金属分别与等质量的溶质质量分数相同的稀硫酸反应,产生氢气的质量与反应时间的函数关系如下图所示.下列相关判断中,正确的是A、C.
A.甲是铁,乙是锌
B.甲是锌,乙是铁
C.图1表示稀硫酸足量,图2表示稀硫酸不足量
D.图1表示金属一定有剩余,图2表示金属一定没有剩余.
分析 (1)根据反应物和生成物及其质量守恒定律可以书写化学方程式.
(2)根据已有的知识进行分析,将不锈钢加工成柔软的金属丝是利用了金属的耐腐蚀性和延展性,据此解答.
(3)胃酸的主要成分是盐酸,能与铁反应;
(4)在金属活动性顺序中,氢前的金属能与酸反应生成氢气,金属的位置越靠前,反应的越剧烈,当酸量不足,酸全部参加反应时,生成的氢气质量相同,当酸足量时,铁生成的氢气质量大于锌生成的氢气的质量.
解答 解:(1)氧化铁和一氧化碳反应生成铁和二氧化碳的化学方程式为:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(2)利用新技术能将不锈钢加工成柔软的金属丝,用它和棉纤维一起编织成性能优良的劳保防护服,这是利用了不锈钢的耐腐蚀性和延展性.故选AB.
(3)胃酸的主要成分盐酸与铁反应生成氢气,化学反应式是:2HCl+Fe=H2↑+FeCl2;
(4)在金属活动性顺序中,氢前的金属能与酸反应生成氢气,金属的位置越靠前,反应的越剧烈,在坐标中斜线越陡,观察现象,甲表示的是铁,乙表示的是锌,故A正确,当酸量不足,酸全部参加反应时,生成的氢气质量相同,当酸足量时,铁生成的氢气质量大于锌生成的氢气的质量,观察图1,甲的反应速率慢,表示的是铁,乙的反应速率快,表示的是锌,甲产生的氢气大于乙生成的氢气,表示酸足量,金属全部参加反应,观察图2,产生的氢气质量相同,表明酸全部参加反应,金属可能有剩余,故选:A、C.
故答案为:
(1)Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;(2)AB;(3)2HCl+Fe=H2↑+FeCl2;(4)A、C.
点评 本题考查了铁的物理性质和化学性质,以及金属的活动性强弱,可以依据已有的知识及金属活动性顺序的意义完成此题.

| A. | 菜刀生锈 | B. | 白磷自燃 | C. | 矿石粉碎 | D. | 牛奶变酸 |
 甲、乙两种固体物质的溶解度曲线如图2所示.现将两支分别装有甲、乙两物质饱和溶液的试管(底部均有少量未溶解的固体)浸入盛有水的烧杯里,然后向烧杯中加入适量的氢氧化钠固体,搅拌至完全溶解(如图1),此时对相应变化的判断正确的是( )
甲、乙两种固体物质的溶解度曲线如图2所示.现将两支分别装有甲、乙两物质饱和溶液的试管(底部均有少量未溶解的固体)浸入盛有水的烧杯里,然后向烧杯中加入适量的氢氧化钠固体,搅拌至完全溶解(如图1),此时对相应变化的判断正确的是( )| A. | 甲溶液可能变成不饱和溶液 | |
| B. | 盛乙的试管中未溶解的固体质量减少 | |
| C. | 甲、乙两物质的溶解度都增大 | |
| D. | 乙溶液中溶质质量分数减小 |

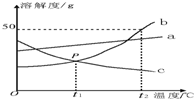 根据如图中a、b、c三种物质的溶解度曲线,回答下列问题:
根据如图中a、b、c三种物质的溶解度曲线,回答下列问题:
 铜、铁、铝作为金属材料一直被广泛应用.
铜、铁、铝作为金属材料一直被广泛应用.