题目内容
1. 现有一份赤铁矿样品(所含杂质不溶于水也不与酸反应),善洁同学要测定其纯度.称取一定量的该样品,向样品中加入19.6%的稀硫酸溶液,固体样品的质量随加入稀硫酸的质量变化关系如图所示.试回答下列问题:
现有一份赤铁矿样品(所含杂质不溶于水也不与酸反应),善洁同学要测定其纯度.称取一定量的该样品,向样品中加入19.6%的稀硫酸溶液,固体样品的质量随加入稀硫酸的质量变化关系如图所示.试回答下列问题:(1)发生反应的化学方程式为Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;
(2)列出样品中参加反应的物质质量(X)的比例式$\frac{160}{x}=\frac{294}{29.4g}$;
(3)若用98%的浓硫酸配制恰好完全反应时所需的上述稀硫酸,需加入水的体积为120mL;
(4)若在恰好完全反应时即停止加入稀硫酸,向最终所得的溶液中加入34g水,则最终所得的溶液中溶质与溶剂的最简比为4:15;
(5)用200t该矿石可制得含杂质的铁的质量是112t.
分析 根据图示结合氧化铁和硫酸的反应进行分析解答,氧化铁能与硫酸反应生成硫酸铁和水,剩余固体是不参与反应的杂质,根据硫酸的质量即可求出参加反应的氧化铁的质量,根据硫酸稀释前后溶质质量不变解答.
解答 解:(1)氧化铁能与硫酸反应生成硫酸铁和水,故填:Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;
(2)硫酸的质量为:150g×19.6%=29.4g
设氧化铁的质量为x
Fe2O3+3H2SO4=Fe2(SO4)3+3H2O
160 294
x 29.4g
$\frac{160}{x}=\frac{294}{29.4g}$,故填:$\frac{160}{x}=\frac{294}{29.4g}$;
(3)设98%的浓硫酸的质量为y,则有98%y=29.4g y=30g,则水的质量为150g-30g=120g,故水的体积为:120g÷1g/mL=120mL,故填:120;
(4)设生成的硫酸铁的质量为z,则有:
Fe2O3+3H2SO4=Fe2(SO4)3+3H2O
294 400
29.4g z
$\frac{294}{29.4g}=\frac{400}{z}$ z=40g
最终所得的溶液中加入34g水,则最终所得的溶液中水的质量为:150g+16g-40g+34g=150g,故最终所得的溶液中溶质与溶剂的最简比为:40g:150g=4:15,故填:4:15;
(5)炼得含杂质的铁的质量为:200t×$\frac{16g}{16g+4g}$×$\frac{56×2}{56×2+16×3}$=112t,故填:112t.
点评 本题考查的是根据化学方程式的计算,完成此题,可以依据已有的知识结合图示进行.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案
相关题目
12.物质的构成与分类
(1)世界上的物质都是由元素组成的,而物质又是由原子、分子和离子等基本粒子构成的.在宏观物质--微观构成--符号之间建立联系,是化学学科特有的思维方式.现有氢、碳、氧、钠、铜、氯六种元素,请按要求填写表中的空白:
(2)分类法是科学研究的一种重要方法,分类标准有多种,化学上可从不同的角度对物质进行分类.请按要求完成下列问题:
Ⅰ.下列两组物质中均有一种物质所属类别与其它两种不同,请指出你的分类标准,并选出该物质,用化学式表示,说明选择的理由.
①烧碱、硫酸铜、熟石灰:
你的分类标准是根据物质的性质不同;选出的物质是CuSO4,理由是硫酸铜属于盐,其它两种是碱.
②硫酸、氯酸钾、二氧化碳:
你的分类标准是根据物质的组成元素不同;选出的物质是CO2,理由是二氧化碳由2种元素组成,其它两种由3种元素组成.
Ⅱ.以构成物质粒子的种类不同为分类标准,将水、铁、金刚石三种物质进行分类,其中不同类的物质是(用化学式表示)H2O,理由是水是由分子构成的,铁和金刚石是由原子构成的.
(1)世界上的物质都是由元素组成的,而物质又是由原子、分子和离子等基本粒子构成的.在宏观物质--微观构成--符号之间建立联系,是化学学科特有的思维方式.现有氢、碳、氧、钠、铜、氯六种元素,请按要求填写表中的空白:
| 编号 | 组成物质的要求 | 物质的名称 | 物质的化学式 | 构成物质的粒子 (用化学符号表示) |
| 示例 | 一种气体单质 | 氧气 | O2 | O2 |
| ① | 常做导线的一种金属单质 | |||
| ② | 由三种元素组成的 一种可溶性盐 | |||
| ③ | 由三种元素组成的有机物,可作燃料 |
Ⅰ.下列两组物质中均有一种物质所属类别与其它两种不同,请指出你的分类标准,并选出该物质,用化学式表示,说明选择的理由.
①烧碱、硫酸铜、熟石灰:
你的分类标准是根据物质的性质不同;选出的物质是CuSO4,理由是硫酸铜属于盐,其它两种是碱.
②硫酸、氯酸钾、二氧化碳:
你的分类标准是根据物质的组成元素不同;选出的物质是CO2,理由是二氧化碳由2种元素组成,其它两种由3种元素组成.
Ⅱ.以构成物质粒子的种类不同为分类标准,将水、铁、金刚石三种物质进行分类,其中不同类的物质是(用化学式表示)H2O,理由是水是由分子构成的,铁和金刚石是由原子构成的.
9.下列关于碳和碳的氧化物的说法不正确的是( )
| A. | C和CO都可以将CuO中的Cu置换出来 | |
| B. | 在一定条件下CO2与CO可以相互转化 | |
| C. | 金刚石、石墨和C60都属于碳单质、但物理性质差异很大 | |
| D. | 温室效应既可以体现CO2的功,又可以体现CO2的过 |
6.下列变化中,前者是化学变化,后者是物理变化的是( )
| A. | 轮胎爆炸、百炼成钢 | B. | 食物腐败、干冰升华 | ||
| C. | 钢铁生锈、庄稼长高 | D. | 工业制氧、石墨转化为金刚石 |
13. 如图所示是镁元素在元素周期表中的信息和该原子的原予结构示意图,据此判断,下列说法不正确的是( )
如图所示是镁元素在元素周期表中的信息和该原子的原予结构示意图,据此判断,下列说法不正确的是( )
 如图所示是镁元素在元素周期表中的信息和该原子的原予结构示意图,据此判断,下列说法不正确的是( )
如图所示是镁元素在元素周期表中的信息和该原子的原予结构示意图,据此判断,下列说法不正确的是( )| A. | 镁原子的相对原子质量为24.31 | |
| B. | 在化学反应中,镁原子容易形成阳离子 | |
| C. | 该元素形成的硝酸盐是MgNO3 | |
| D. | 镁原子核内有l 2个质子 |
10.下列数据是相应物质的近似pH,其中一定呈碱性的是( )
| A. |  (6.5-7.5)饮用水 | B. |  (4.0-4.4)番茄汁 | C. |  (2.0-3.0)柠檬汁 | D. |  (9.5-10.5)洗发液 |
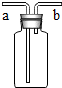 (1)若用如图所示正放的装置收集氧气,则氧气应从a(填“a”或“b”下同)端通入;若用装满水的正放的该装置收集氧气,则氧气应从b端通入;
(1)若用如图所示正放的装置收集氧气,则氧气应从a(填“a”或“b”下同)端通入;若用装满水的正放的该装置收集氧气,则氧气应从b端通入; “格瓦斯”(用面包发酵酿制的碳酸饮料),是以面包提取液、果葡糖浆、啤酒花、白砂糖等物质为原料,经多种乳酸菌、酵母菌复合发酵酿制而成的微醇性生物饮品,具有开胃、健脾、降血压、消除疲劳等保健作用.请回答下列问题:
“格瓦斯”(用面包发酵酿制的碳酸饮料),是以面包提取液、果葡糖浆、啤酒花、白砂糖等物质为原料,经多种乳酸菌、酵母菌复合发酵酿制而成的微醇性生物饮品,具有开胃、健脾、降血压、消除疲劳等保健作用.请回答下列问题: