题目内容
17.学校化学实验室需要配制一定浓度NaCl溶液进行实验,回答下列问题(1)计算:配制20%的NaCl溶液200g,计算需要NaCl的质量和水的体积;
(2)称量:托盘天平称量时发现指针偏向左侧,此时的正确做法是D(填序号)
A、增加砝码 B、调节游码 C、添加药品 D、减少药品
(3)量取:用量筒量取水时,要注意视线和液体凹液面最低处保持水平
(4)溶解:将NaCl与水混合溶液,装瓶贴标签放置,若装瓶过程中有溶液外溅,不会影响溶质的质量分数,原因是溶液具有均一性.
(5)稀释:现取出50g20%的NaCl溶液配制成5%的NaCl溶液,需要加入水的体积是150mL(水的密度为1g•mL-3)
分析 (1)溶质质量=溶液质量×溶质质量分数;
(2)称量时,托盘天平称量时发现指针偏向左侧,说明样品质量偏大,此时的正确做法是减少药品;
(3)用量筒量取水时,要注意视线和液体凹液面最低处保持水平;
(4)溶液具有均一性、稳定性;
(5)溶液稀释前后,溶质质量不变.
解答 解:(1)配制20%的NaCl溶液200g,需要NaCl的质量为:200g×20%=40g,
需要水的体积为:(200g-40g)÷1g/mL=160mL,
答:需要40g氯化钠,160mL的水.
(2)托盘天平称量时发现指针偏向左侧,此时的正确做法是减少药品.
故填:D.
(3)用量筒量取水时,要注意视线和液体凹液面最低处保持水平.
故填:液体凹液面最低处.
(4)若装瓶过程中有溶液外溅,不会影响溶质的质量分数,原因是溶液具有均一性.
故填:溶液具有均一性.
(5)现取出50g20%的NaCl溶液配制成5%的NaCl溶液,需要加入水的体积是:(50g×20%÷5%-50g)÷1g/mL=150mL,
故填:150.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
相关题目
9.空气中体积分数约占21%的气体是( )
| A. | 氮气 | B. | 氧气 | C. | 二氧化碳 | D. | 稀有气体 |
2.下列实验现象描述正确的是( )
| A. | 硫在空气中燃烧发出明亮的蓝紫色火焰 | |
| B. | 电解水的实验中负极产生的气体使带火星的木条复燃 | |
| C. | 打开盛有浓硫酸的试剂瓶,瓶口会产生白雾 | |
| D. | 将充满CO2的试管倒扣在石蕊溶液中,试管内液面上升且变为红色 |
6. 某海洋化工集团用氨碱法生产的纯碱产品中含有少量氯化钠杂质.其产品包装袋上注明:碳酸钠≥96%.为测定该产品中含碳酸钠的质量分数,进行了以下实验:取11.00g纯碱样品放入烧杯中,称得烧杯及所盛纯碱样品的总质量为158.00g,再把100.00g稀盐酸平均分成四份依次加入样品中,实验数据记录如下:
某海洋化工集团用氨碱法生产的纯碱产品中含有少量氯化钠杂质.其产品包装袋上注明:碳酸钠≥96%.为测定该产品中含碳酸钠的质量分数,进行了以下实验:取11.00g纯碱样品放入烧杯中,称得烧杯及所盛纯碱样品的总质量为158.00g,再把100.00g稀盐酸平均分成四份依次加入样品中,实验数据记录如下:
(1)分析表中数据数据X的值是204.48.
(2)请你通过计算说明该产品中碳酸钠的质量分数是否合格?(要求写出计算过程,结果精确到0.1%)
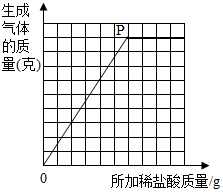
(3)根据实验数据,某同学在坐标纸上绘制出了所加稀盐酸质量与生成气体质量关系的曲线请你求出图中转折处P点的坐标.(保留一位小数)
 某海洋化工集团用氨碱法生产的纯碱产品中含有少量氯化钠杂质.其产品包装袋上注明:碳酸钠≥96%.为测定该产品中含碳酸钠的质量分数,进行了以下实验:取11.00g纯碱样品放入烧杯中,称得烧杯及所盛纯碱样品的总质量为158.00g,再把100.00g稀盐酸平均分成四份依次加入样品中,实验数据记录如下:
某海洋化工集团用氨碱法生产的纯碱产品中含有少量氯化钠杂质.其产品包装袋上注明:碳酸钠≥96%.为测定该产品中含碳酸钠的质量分数,进行了以下实验:取11.00g纯碱样品放入烧杯中,称得烧杯及所盛纯碱样品的总质量为158.00g,再把100.00g稀盐酸平均分成四份依次加入样品中,实验数据记录如下:| 所加盐酸的次数 | 第一次 | 第二次 | 第三次 | 第四次 |
| 每次加盐酸前 烧杯及所盛物质的总质量/g | 158.00 | 181.24 | X | 228.60 |
| 所加盐酸的溶液质量/g | 25.00 | 25.00 | 25.00 | 25.00 |
| 充分反应后烧杯及所盛物质总质量/g | 181.24 | 204.48 | 228.60 | 253.60 |
| 每次生成的二氧化碳质量/g | 1.76 | 1.76 | Y | 0 |
(2)请你通过计算说明该产品中碳酸钠的质量分数是否合格?(要求写出计算过程,结果精确到0.1%)
(3)根据实验数据,某同学在坐标纸上绘制出了所加稀盐酸质量与生成气体质量关系的曲线请你求出图中转折处P点的坐标.(保留一位小数)
7.2012年2月某地发生了一起亚硝酸钠中毒事件.亚硝酸钠外观酷似食盐且有咸味,亚硝酸钠和食盐的有关资料如下:
根据上表提供的信息完成下列问题:
(1)写出亚硝酸钠的两条物理性质:易溶于水,熔点271℃.
(2)请你写出检验食盐中是否含有亚硝酸钠的过程(操作、现象、结论):取少量待测食盐与稀盐酸反应,若有红棕色气体产生,则该食盐中混有亚硝酸钠,反之则无;(或取待测食盐加热到320℃以上,若有臭味气体产生,则食盐中含有亚硝酸钠,反之则无).
| 项 目 | 亚硝酸钠(NaNO2) | 氯化钠(NaCl) |
| 水溶性 | 易溶,在15℃时溶解度为81.5克 | 易溶,在15℃时溶解度为35.8克 |
| 熔点 | 271℃ | 801℃ |
| 沸点 | 320℃会分解,放出有臭味的气体 | 1413℃ |
| 跟稀盐酸作用 | 放出红棕色的气体NO2 | 无反应 |
(1)写出亚硝酸钠的两条物理性质:易溶于水,熔点271℃.
(2)请你写出检验食盐中是否含有亚硝酸钠的过程(操作、现象、结论):取少量待测食盐与稀盐酸反应,若有红棕色气体产生,则该食盐中混有亚硝酸钠,反之则无;(或取待测食盐加热到320℃以上,若有臭味气体产生,则食盐中含有亚硝酸钠,反之则无).