题目内容
7.在一只密闭容器内有四种物质,在一定条件下充分反应,测得反应前后各物质的质量如表:| 物质 | X | Y | Z | Q |
| 反应前质量/g | 8 | 2 | 40 | 5 |
| 反应后质量/g | 待测 | 24 | 8 | 23 |
| A. | 该反应一定是分解反应 | B. | Y、Q的相对分子质量比一定为11:9 | ||
| C. | 反应后X的质量为0 | D. | 在反应中X和Z的质量比为1:5 |
分析 此题是借助质量守恒定律对反应物生成物先做出判断,再利用质量关系进行求解.反应中反应物质量会减少,生成物质量会增加,从而判断生成物与反应物,即可判断反应的类型.根据反应物与生成物质量相等可求出待测的质量、各物质的质量比等.
解答 解:由表中数据看出反应后Z的质量减少了32g,属于反应物,Y和Q的质量增加,属于生成物,分别生成了22g和18g,由质量守恒定律可知,x属于反应物应且参加了22g+18g-32g=8g,故待测为0;有由此可知:
A、由表中的数据,该反应反应物是两种生成物是两种,所以该反应一定不是分解反应,故A错误;
B、由表中的数据,可以求出Y、Q的质量比为22g:18g11:9,故B正确;
C、反应后X的质量为8g-8g=0,故C正确;
D、参加反应的X、Z的质量比为:8g:32g=1:4,故D不正确.
故选BC.
点评 根据质量守恒定律,密封容器内各物质质量总和在反应前后相等,是解决此类问题的技巧.

练习册系列答案
相关题目
17.下列除杂(括号中物质为杂质)所用的试剂或方法正确的是( )
| A. | KNO3(NaCl):蒸发结晶 | |
| B. | CO(CO2):点燃 | |
| C. | FeSO4溶液(CuSO4溶液):过量的铁,过滤 | |
| D. | CaCO3(CaCl2):溶解,过滤,蒸发结晶 |
18.比较、推理是化学学习常用的方法.以下是根据一些反应事实推导出的影响化学反应的因素,其中不合理的是( )
| 化学反应事实 | 影响反应的因素 | |
| A | 铁丝在空气中很难燃烧,在氧气中能剧烈燃烧 | 反应物的浓度 |
| B | 碳在常温下不与氧气反应,在点燃时能与氧气反应 | 反应的温度 |
| C | 过氧化氢在常温下较难分解,在加入二氧化锰后迅速分解 | 催化剂 |
| D | 铜片在空气中很难燃烧,铜粉在空气中较易燃烧 | 反应物的种类 |
| A. | A | B. | B | C. | C | D. | D |
2.(1)A~F是初中化学中的常见物质,如图所示是它们之间的转化关系,图中部分反应物或生成物未全部标出.已知:A是天然气的主要成分,B在常温下为液态,F是黑色粉末.

①A物质的化学式为CH4;
②B→D是放热反应(填“放热”或“吸热”);
③在C→E的反应中,C物质发生还原反应(填“氧化反应”或“还原反应”);
④写出E→F反应的化学方程式:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(2)设计对比实验,控制变量是学习化学的重要方法,下列对比实验不能达到目的是B.

①A物质的化学式为CH4;
②B→D是放热反应(填“放热”或“吸热”);
③在C→E的反应中,C物质发生还原反应(填“氧化反应”或“还原反应”);
④写出E→F反应的化学方程式:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(2)设计对比实验,控制变量是学习化学的重要方法,下列对比实验不能达到目的是B.
| 编号 | A | B |
| 实验设计 |  |  |
| 实验目的 | 探究同种物质在不同溶剂中的溶解性 | 探究MnO2对过氧化氢分解的影响 |
12.某工化肥厂需大量二氧化碳生产化肥,欲购进一批石灰石(其中杂质不参加任何反应),厂家到产地取样分析以确定价格.他们取样2克,并把20克稀盐酸分四次加入,充分反应后,每次剩余固体质量见表
试计算:
(1)2克石灰石样品中含有杂质的质量是0.4克.
(2)石灰石样品中碳酸钙的质量分数是多少?
(3)1000千克这种石灰石充分煅烧后,可得二氧化碳质量是多少?( CaCO3$\frac{\underline{\;高温\;}}{\;}$ CaO+CO2↑ )
| 稀盐酸的用量 | 剩余固体的质量/g |
| 第一次加入5g | 1.4g |
| 第二次再加入5g | 0.8g |
| 第三次再加入5g | 0.4g |
| 第四次再加入5g | 0.4g |
(1)2克石灰石样品中含有杂质的质量是0.4克.
(2)石灰石样品中碳酸钙的质量分数是多少?
(3)1000千克这种石灰石充分煅烧后,可得二氧化碳质量是多少?( CaCO3$\frac{\underline{\;高温\;}}{\;}$ CaO+CO2↑ )
19.根据化学方程式Na2CO3+2A═H2O+2B+CO2↑,推断B、A的相对分子质量差为( )
| A. | 44 | B. | 33 | C. | 22 | D. | 11 |
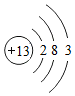 (1)用正确的化学用语填空:
(1)用正确的化学用语填空: 表示的微粒是Cl.
表示的微粒是Cl.