题目内容
16.实验是学习化学的重要途径,请根据如图实验装置和仪器,回答问题:
(1)标号①的仪器名称:长颈漏斗
(2)请写出实验室用高锰酸钾制取氧气的化学方程式2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,先用K装置收集气体时,下列实验操作正确的是①②③(填序号)
①反应前,将集气瓶注满水,用玻璃片盖着瓶口,倒立在盛水的水槽中.
②开始反应后,等到气泡连续且均匀时,再将导管口移入集气瓶
③收集气体时,将集气瓶盖上玻璃片再移出水槽
实验过程中,发现装置K中的水变为红色,为了防止此现象的发生,改进措施是A装置中的试管口放一团棉花,为测定一定量的高锰酸钾分解生成氧气的体积,应选用如上述装置丙(填编号,下同).
(3)若取用一定浓度的盐酸与石灰石反应制取气体,将生成的气体缓慢通入澄清石灰水中,未见变浑浊.为探究其原因,进行了如下过程:
作出猜想:A.石灰水已经完全变质; B.气体中有挥发出来的HCl气体.
实验探究:
①取少量石灰水于试管中,并向试管中滴加几滴无色酚酞试液,振荡,观察到溶液变红色.于是排除了猜想A,你认为排除猜想A的理由是酚酞试液变红,说明溶液中存在碱性物质Ca(OH)2.上述装置中的数字标号②仪器,也可用H代替.
②为了探究所得气体中是否有挥发出来的HCl气体,设计如下实验.
| 实验步骤 | 实验现象 | 实 验结论 |
| 将生成的气体通入硝酸银溶液中 | 产生白色沉淀 | 气体中有HCl |
碳酸钠溶液中通入二氧化碳发生反应:Na2CO3+CO2+H2O═2NaHCO3
拓展延伸:
如果用上述原料通过控制反应速率制取纯净的二氧化碳气体,所选仪器的连接顺序为CGDI(填字母).
分析 (1)根据实验室常用仪器的名称和题中所指仪器的作用进行分析;
(2)根据高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,以及实验室用排水法收集氧气的正确操作进行分析;
根据实验室用高锰酸钾制取时,需要在试管口放一团棉花,防止高锰酸钾粉末进入导管,为测定一定量的高锰酸钾分解生成氧气的体积,应短进长出进行分析;
(3)【实验探究】①根据氢氧化钙溶液显碱性,能使酚酞变红色进行分析;
②根据氯离子和银离子会生成氯化银沉淀进行分析;
【拓展延伸】根据实验室制取二氧化碳的反应物是固体和液体,反应条件生成物,生成的二氧化碳中含有氯化氢气体、水蒸气,二氧化碳与氢氧化钠、碳酸钠溶液可反应,所以需要先用碳酸氢钠溶液将氯化氢除去,再用浓硫酸干燥,然后用向上排空气法收集二氧化碳进行分析.
解答 解:(1)通过分析题中所指仪器的作用可知,①是长颈漏斗;
(2)高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,
①反应前,将集气瓶注满水,用玻璃片盖着瓶口,倒立在盛水的水槽中,故正确
②开始反应后,等到气泡连续且均匀时,再将导管口移入集气瓶,故正确;
③收集气体时,将集气瓶盖上玻璃片再移出水槽,故正确;
故选:①②③;
实验室用高锰酸钾制取时,需要在试管口放一团棉花,防止高锰酸钾粉末进入导管,为测定一定量的高锰酸钾分解生成氧气的体积,应短进长出,故选:丙;
(3)【实验探究】①氢氧化钙溶液显碱性,碱能使酚酞变红色,所以排除猜想A的理由是:酚酞试液变红,说明溶液中存在碱性物质Ca(OH)2,上述装置中的数字标号②仪器,也可用H代替;
②据实验结论可知:气体中有挥发出来的HCl气体,氯化氢溶于水形成盐酸,会与硝酸银溶液反应生成白色的氯化银沉淀;
【拓展延伸】实验室制取二氧化碳的反应物是固体和液体,属于固液常温型,则选发生装置B,生成的二氧化碳中含有氯化氢气体、水蒸气,由资料可知:二氧化碳可与碳酸钠溶液反应,且二氧化碳也可与氢氧化钠溶液反应,所以实验须先用碳酸氢钠溶液将氯化氢除去,再用浓硫酸干燥,二氧化碳密度比空气大,然后用向上排空气法收集二氧化碳,所选仪器的连接顺序为CGDI.
故答案为:(1)长颈漏斗;
(2)2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,①②③;在试管口放一团棉花,丙;
(3)【实验探究】①酚酞试液变红,说明溶液中存在碱性物质Ca(OH)2,②;
②硝酸银,生成白色沉淀;
【拓展延伸】CGDI.
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.

 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案| A. | 向右偏 | B. | 向左偏 | C. | 保持平衡 | D. | 无法确定 |
| A. | 氮气常用作保护气--氮气化学性质稳定 | |
| B. | 固体二氧化碳可用人工降雨--二氧化碳能与碱反应 | |
| C. | 氢氧化钙可用来改良酸性土壤--氢氧化钙溶液呈碱性 | |
| D. | 氧化钙可做食品干燥剂--氧化钙能与水反应 |
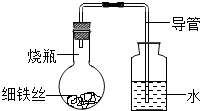 小明同学为了研究影响铁生锈的因素,进行了如下实验:
小明同学为了研究影响铁生锈的因素,进行了如下实验:在A、B、C、D四只烧瓶中分别放入干燥的细铁丝、浸过食盐水的细铁丝、浸过清水的细铁丝、食盐水及细铁丝(使细铁丝完全浸没在食盐水中)(四只烧瓶中细铁丝的质量均相同),然后装配成如图所示的四套装置,每隔0.5小时测量导管中水面上升的高度,结果如下表所示:
| 烧瓶号 | 时间/h 导管中水面上升高度/cm | 0 | 0.5 | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 |
| A瓶 | 盛干燥的细铁丝 | 0 | 0 | 0 | 0 | 0 | 0 | 0 |
| B瓶 | 盛浸过食盐水的细铁丝 | 0 | 0.4 | 1.2 | 3.4 | 5.6 | 7.6 | 9.8 |
| C瓶 | 盛浸过清水的细铁丝 | 0 | 0 | 0 | 0.3 | 0.8 | 2.0 | 3.5 |
| D瓶 | 盛完全浸没在食盐水中的细铁丝 | 0 | 0 | 0 | 0 | 0 | 0 | 0 |
(1)以上实验中,铁生锈的速率最大的是B(填烧瓶号).
(2)导管中水面上升的原因是烧瓶中的氧气参加反应,气体减少,压强降低.
(3)以上实验说明,影响铁生锈的因素是水和氧气,食盐能够促进铁生锈.
(4)为了防止钢铁锈蚀,人们常采用在其表面涂刷矿物油或镀上其他金属等覆盖保护膜的方法,这些方法的共同原理是隔绝氧气和水.
| A. | 磷在空气中燃烧产生大量白烟 | |
| B. | 在电解水实验中,正负两极产生的气体体积比约为2:1 | |
| C. | 打开盛有浓盐酸的试剂瓶,看到瓶口有大量白雾 | |
| D. | 取少量氢氧化钠暴露在空气中,氢氧化钠表面潮湿并逐渐溶解 |

 如图是常见干电池的剖面图,据此回答下列问题.
如图是常见干电池的剖面图,据此回答下列问题.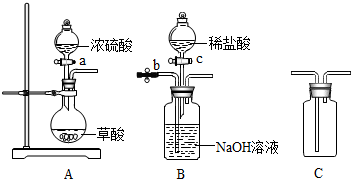 豆腐不可与菠菜一起煮,原因是菠菜含有丰富的草酸、草酸钠,豆腐中含有较多的硫酸钙等钙盐,相互反应生成草酸钙沉淀等物质.其中发生的反应属于D(填选项字母).
豆腐不可与菠菜一起煮,原因是菠菜含有丰富的草酸、草酸钠,豆腐中含有较多的硫酸钙等钙盐,相互反应生成草酸钙沉淀等物质.其中发生的反应属于D(填选项字母).