题目内容
15. 实验室可用高锰酸钾、双氧水和二氧化锰来制取氧气.
实验室可用高锰酸钾、双氧水和二氧化锰来制取氧气.(1)写出实验室用双氧水和二氧化锰制取氧气的化学方程式:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(2)若实验室用高锰酸钾为药品制取氧气并收集一瓶氧气,实验时应选择图中A和D装置(填字母)来制取和收集.
(3)如何检验集气瓶中的O2已经收集满(填操作和现象)?
答:将带火星的木条放在集气瓶口,木条复燃,证明集满.
(4)开展探究:为检验木炭在氧气中燃烧生成CO2:小明用镊子夹住烧红的木炭,伸入充满O2的集气瓶中.充分反应后,往集气瓶中加入适量澄清石灰水,振荡,此时可观察到澄清石灰水变浑浊,反应方程式为Ca(OH)2+CO2=CaCO3↓+H2O.
分析 (1)根据过氧化氢在二氧化锰的催化作用下生成水和氧气进行分析;
(2)根据实验室用高锰酸钾制取氧气的反应物是固体,反应条件是加热,氧气密度比空气大,不易溶于水进行分析;
(3)根据氧气有助燃性进行分析;
(4)根据碳和氧气点燃生成二氧化碳,二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水进行分析.
解答 解:(1)过氧化氢在二氧化锰的催化作用下生成水和氧气,化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(2)实验室用高锰酸钾制取氧气的反应物是固体,反应条件是加热,氧气密度比空气大,不易溶于水,所以实验时应选择图中A和D来制取和收集;
(3)氧气有助燃性,所以验满的操作是:将带火星的木条放在集气瓶口,木条复燃,证明集满;
(4)碳和氧气点燃生成二氧化碳,二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,所以观察到澄清石灰水变浑浊,化学方程式为:Ca(OH)2+CO2=CaCO3↓+H2O.
故答案为:(1)2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(2)A,D;
(3)将带火星的木条放在集气瓶口,木条复燃,证明集满;
(4)澄清石灰水变浑浊,Ca(OH)2+CO2=CaCO3↓+H2O.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.

练习册系列答案
相关题目
3.正确的操作是实验成功的保证.如图所示实验操作正确的是( )
| A. |  | B. |  | C. |  | D. |  |
20.今年,我国北方很多地方旱情比较严重,水资源紧缺,有关部门呼吁,人人都应该树立保护水资源的意识,养成节约用水的习惯,下列做法不利于节约用水的是( )
| A. | 洗菜、淘米的水用来浇花、拖地、冲厕所 | |
| B. | 推广使用节水用品 | |
| C. | 工业废水处理后循环使用 | |
| D. | 洗澡擦肥皂时不关喷头.使水流淌 |
5.下列有关碳和碳的氧化物的说法中不正确的是( )
| A. | 常温下二氧化碳是一种无色无味的有毒气体 | |
| B. | 工业中利用活性炭来脱色以制白糖 | |
| C. | 室内放一盆水不能防止一氧化碳中毒 | |
| D. | CO2可用于灭火,CO可用作燃料 |
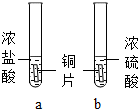 化学课上探究金属的化学性质时,同学们发现铜与稀盐酸、稀硫酸在常温或短时间加热的条件下均不反应.那么,铜与浓盐酸、浓硫酸能否发生反应呢?兴趣小组进行如下探究.
化学课上探究金属的化学性质时,同学们发现铜与稀盐酸、稀硫酸在常温或短时间加热的条件下均不反应.那么,铜与浓盐酸、浓硫酸能否发生反应呢?兴趣小组进行如下探究.